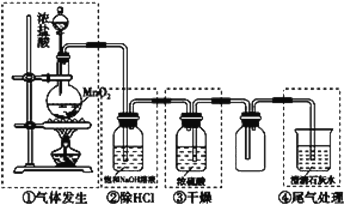
题目内容
【题目】现有2.8gFe全部溶于一定浓度、200ml的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1.若反应前后溶液体积变化忽略不计,则下列有关判断不正确的是
A. 反应后溶液中c(NO3-)=0.85mol/L
B. 反应后的溶液最多还能溶解1.4gFe
C. 反应后溶液中铁元素可能以Fe3+形式存在
D. 1.12L气体只能是NO
【答案】B
【解析】
A.反应后溶液为硝酸铁、硝酸的混合溶液,故溶液中有3c(Fe3+)+c(H+)=c(NO3-),根据铁元素守恒由n(Fe)=n(Fe3+)=0.05mol,所以c(Fe3+)=![]() =0.25mol/L,反应后溶液pH为1,所以c(H+)=0.1mol/L,所以c(NO3-)=0.25mol/L×3+0.1mol/L=0.85mol/L,选项A正确;
=0.25mol/L,反应后溶液pH为1,所以c(H+)=0.1mol/L,所以c(NO3-)=0.25mol/L×3+0.1mol/L=0.85mol/L,选项A正确;
B.由A中分析可知,原硝酸是稀硝酸,反应生成NO,由氮元素守恒可知n原来(HNO3)=3n[Fe(NO3)2]+n剩余(HNO3)+n(NO)=0.05mol×3+0.1mol/L×0.2+0.05mol=0.22mol,生成Fe(NO3)2、NO时原硝酸溶解的铁最多,由3Fe+8HNO3=3Fe(NO3)2+2 NO↑+4H2O 可知,0.22molHNO3最多溶解铁![]() ×0.22mol,质量为
×0.22mol,质量为![]() ×0.22mol×56g/mol=4.62g,故还能溶解铁4.64g-2.8g=1.82g,选项B不正确;
×0.22mol×56g/mol=4.62g,故还能溶解铁4.64g-2.8g=1.82g,选项B不正确;
C.反应后溶液pH为1,故HNO3过量,Fe只可能转化为Fe3+,选项C正确;
D.2.8gFe的物质的量为![]() =0.05mol,若只生成NO,根据电子转移守恒可知,n(NO)=
=0.05mol,若只生成NO,根据电子转移守恒可知,n(NO)=![]() =0.05mol,则V(NO)=0.05mol×22.4L/mol=1.12L;若只生成NO2,根据电子转移守恒可知,n(NO2)=
=0.05mol,则V(NO)=0.05mol×22.4L/mol=1.12L;若只生成NO2,根据电子转移守恒可知,n(NO2)=![]() =0.15mol,V(NO2)=0.15mol×22.4L/mol=3.36L,由于实际生成气体1.12L,故只生成NO, 选项D正确;
=0.15mol,V(NO2)=0.15mol×22.4L/mol=3.36L,由于实际生成气体1.12L,故只生成NO, 选项D正确;
答案选B。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子排布图为_____________
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______。
(3)部分电离能数据如下表:
元素 | Mn | Fe | |
电离能 |
| 717 | 759 |
| 1 509 | 1 561 | |
| 3 248 | 2 957 | |
根据表中数据可知,气态![]() 再失去一个电子比气态
再失去一个电子比气态![]() 再失去一个电子难,其原因是___________________________。
再失去一个电子难,其原因是___________________________。
(4)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合“18电子规则”。如Cr可以与CO形成![]() 分子:价电子总数
分子:价电子总数![]() 的价电子数
的价电子数![]() 提供电子数
提供电子数![]() .Fe原子也能与CO形成配合物,其化学式为________.
.Fe原子也能与CO形成配合物,其化学式为________.
(5)已知Fe单质有如图所示的两种常见堆积方式:


其中属于体心立方密堆积的是______![]() 填“a”或“b”
填“a”或“b”![]() ;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
(6)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3。
【题目】一般较强酸可制取较弱酸,这是复分解反应的规律之一。已知在常温下测得浓度均为0.1mol/L的下列 3 种溶液的 pH:
溶质 | NaHCO3 | Na2CO3 | NaClO |
pH | 8.34 | 11.6 | 10.3 |
下列有关说法正确的是( )
A. 以上溶液的 pH 是用广泛 pH 试纸测定的
B. 反应CO2+H2O+2NaClO=Na2CO3+2HClO可以发生
C. 室温下,电离常数: K2( H2CO3)>K( HClO)
D. 在新制氯水中加入少量 NaHCO3固体可以提高溶液中 HClO 的浓度