题目内容
【题目】铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子排布图为_____________
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______。
(3)部分电离能数据如下表:
元素 | Mn | Fe | |
电离能 |
| 717 | 759 |
| 1 509 | 1 561 | |
| 3 248 | 2 957 | |
根据表中数据可知,气态![]() 再失去一个电子比气态
再失去一个电子比气态![]() 再失去一个电子难,其原因是___________________________。
再失去一个电子难,其原因是___________________________。
(4)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合“18电子规则”。如Cr可以与CO形成![]() 分子:价电子总数
分子:价电子总数![]() 的价电子数
的价电子数![]() 提供电子数
提供电子数![]() .Fe原子也能与CO形成配合物,其化学式为________.
.Fe原子也能与CO形成配合物,其化学式为________.
(5)已知Fe单质有如图所示的两种常见堆积方式:


其中属于体心立方密堆积的是______![]() 填“a”或“b”
填“a”或“b”![]() ;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
(6)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3。
【答案】![]() CO2或N2O等合理答案 Mn2+3d能级为半充满结构,较稳定,不易失去电子。 Fe(CO)5 b
CO2或N2O等合理答案 Mn2+3d能级为半充满结构,较稳定,不易失去电子。 Fe(CO)5 b ![]() pm
pm ![]()
【解析】
(1)铁是26号元素,其原子核外有26个电子,Fe原子的3d、4s电子为其价电子,根据构造原理书写Fe核外价电子排布式;
(2)原子个数相等且价电子数相等的分子或离子为等电子体;
(3)Mn2+的价电子为3d5,3d轨道半充满,较稳定;Fe2+的价电子为3d6,不稳定;
(4)铁元素,价电子数为8,根据18电子规则,它可以结合5个CO形成配合物;
(5)由晶胞示意图可知,a为面心立方最密堆积,b为体心立方最密堆积,若单质Fe按a方式紧密堆积,Fe原子的半径为rpm,故晶胞棱长为![]() pm;
pm;
(6)根据密度ρ=m/V进行计算。
(1)Fe是26号元素,其原子核外有26个电子,铁原子失去2个电子生成Fe2+,其3d轨道上6个电子为其外围电子,其价层电子排布图为![]() ,故答案为:
,故答案为:![]() 。
。
(2)SCN-中含有3个原子,且其价电子数是16,与SCN-互为等电子体的一种分子为CO2、N2O、CS2、COS等,故答案为:CO2、N2O、CS2、COS等合理答案。
(3)Mn元素为25号元素,价电子的排布式为:3d54s2;Mn2+的价电子为3d5,3d轨道半充满,较稳定,由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;Fe2+的价电子为3d6,不稳定,由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少,故答案为:Mn2+3d能级为半充满结构,较稳定,不易失去电子。
(4)铁元素,价电子数为8,每个配体提供的电子数是2,8+2n=18,n=5,它可以结合5个CO形成配合物,所以铁元素形成的配合物的化学式为Fe(CO)5,故答案为:Fe(CO)5。
(5)由晶胞示意图可知,a为面心立方最密堆积,b为体心立方最密堆积,若单质Fe按a方式紧密堆积,Fe原子的半径为rpm,故晶胞棱长为![]() pm,故答案为:b;
pm,故答案为:b;![]() pm。
pm。
(6)根据晶胞结构可知含有铁原子的个数为12×1/4+1=4,硫原子个数为8×1/8+6×1/2=4,晶胞边长为anm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为ρ=m/V=![]() g/cm3,故答案为:
g/cm3,故答案为: ![]() 。
。

【题目】某同学通过实验研究Na2O2与水的反应。
操作 | 现象 |
向盛有少量Na2O2的试管中加入蒸馏水,得到溶液a | 反应剧烈,产生能使带火星木条复燃的气体 |
然后向溶液a中滴入两滴酚酞 | 溶液先变红,再逐渐变浅,约10分钟溶液变为无色 |
为了探究溶液变为无色的原因,该同学按照科学的程序,进行了如下实验:
(推理与假设)
Na2O2与H2O反应的化学方程式_____。向溶液a中滴加酚酞本应只会变红,而实验中发现酚酞变红后又褪色。由此提出如下的假设:
假设A:O2有漂白性 假设B:NaOH有漂白性 假设C:O2和NaOH共同作用有漂白性
(实验与观察)
(2)请完成下表:
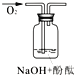
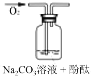
实验编号 | 1 | 2 | 3 |
实验装置 |
|
|
|
实验假设 (填“A”、“B”或“C”) | 假设_____ | 假设____ | 假设__ |
实验现象 | 溶液变红后10分钟均无变化 | ||
实验结论 | _____ | ||
(查阅资料)
该同学查阅资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
(推理与假设)
该同学认为褪色的原因可能是溶液a中存在H2O2,H2O2漂白了酚酞。
(实验与观察)
(3)通过实验证实了H2O2的存在:取少量溶液a,加入黑色粉末____(填化学式),快速产生了能使带火星木条复燃的气体。该同学进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应。实验方案:取少量溶液a于试管中,_____。
(解释与结论)
(4