题目内容
将1mol Fe(OH)3制成胶体,所得胶体中分散质的物质的量 1mol.(填“大于”、“小于”或“等于”)
考点:胶体的重要性质
专题:溶液和胶体专题
分析:胶体分散质微粒直径的大小在1nm~100nm之间,所以胶粒由若干个Fe(OH)3分子构成的一个集合体,据此分析解答.
解答:
解:Fe(OH)3胶体的胶粒是许多Fe(OH)3微粒的聚集体,Fe(OH)3胶体中,将1mol Fe(OH)3制成胶体,所得胶体中分散质的物质的量小于1mol,
故答案为:小于;
故答案为:小于;
点评:本题主要考查胶体的胶粒的构成,注意胶体分散质微粒直径的大小在1nm~100nm之间是解答本题的关键,题目较简单.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
天然气、石油、煤等在地球上的蕴藏量是有限的,则下列说法正确的是( )
①可利用电解水的方法制得氢气作能源
②可砍伐树木、野草作能源
③应开发太阳能、核能等新能源,大量应用风能、水能等可再生能源.
①可利用电解水的方法制得氢气作能源
②可砍伐树木、野草作能源
③应开发太阳能、核能等新能源,大量应用风能、水能等可再生能源.
| A、① | B、② | C、②③ | D、③ |
下列有关金属的工业制法中,正确的是( )
| A、制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B、制铁:以铁矿石为原料,用焦炭和空气反应生成CO在高温下还原铁矿石中的铁 |
| C、制镁:用海水为原料,经一系列过程制得氧化镁固体,电解熔融的氧化镁得镁 |
| D、制钛:用金属钠置换TiCl4溶液中的钛 |
下列反应的离子方程式书写正确的是( )
| A、FeS固体溶于稀HNO3:FeS+2H+=Fe2++H2S↑ |
| B、AlCl3和过量氨水反应:Al3++3OH-=Al(OH)3↓ |
| C、向AgCl悬浊液中滴加硫化钠溶液,白色沉淀变成黑色:2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-(aq) |
| D、体积等浓度的NaHSO4与Ba(0H)2溶液混合:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
下列说法正确的是( )
| A、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C、一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D、相同条件下,溶液中Cu2+、Fe3+、Zn2+的氧化性依次增强 |
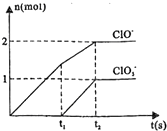 已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示.
已知NaOH与Cl2反应的氧化产物与温度有关(发生的反应均为放热反应),在V L 4mol/L的NaOH中通入一定量的氯气,生成物中含有Cl-、ClO-、ClO3-三种含氯元素的离子,其中C1O-、ClO3-的物质的量(n)与反应时间(t)的曲线如图所示.