题目内容
【题目】Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素 | 相关信息 |
Y | 原子核外有6个不同运动状态的电子 |
Z | 非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同 |
W | 主族元素,与Z原子的价电子数相同 |
R | 价层电子排布式为3d64s2 |
M | 位于第ⅠB族,其被称作“电器工业的主角” |
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是____,M2+的核外电子排布式为_______。
(2)M2Z的熔点比M2W的______(填“高”或“低”),请解释原因:_____________。
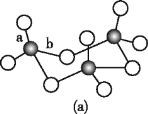
(3)WZ2的VSEPR模型名称为______;WZ3气态为单分子,该分子中W原子的杂化轨道类型为____;WZ3的三聚体环状结构如图(a)所示,该结构的分子中含有____个σ键;写出一种与WZ3互为等电子体的分子的化学式_____。
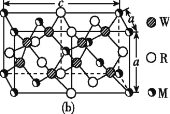
(4)MRW2的晶胞如图(b)所示,晶胞参数a=0.524 nm、c=1.032 nm;MRW2的晶胞中,晶体密度ρ=____g/cm3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA=6.02×1023 mol-1)。
【答案】O [Ar]3d9或1s22s22p63s23p63d9 高 氧离子半径比硫离子半径小,Cu2O比Cu2S的晶格能大,所以Cu2O熔点高 平面三角形 sp2 12 BF3等 ![]()
【解析】
Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大。Y的原子核外有6个不同运动状态的电子,Y为C元素; Z是非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同,Z的电子排布式为1s2s22p4,Z为O元素;W是主族元素,与Z原子的价电子数相同,W为S元素;R的价层电子排布式为3d64s2, R为Fe元素;M位于第IB族,其被称作“电器工业的主角”,为Cu元素,据此分析结合元素性质解答。
(1) Z为O元素,W为S元素,同一主族,从上到下,第一电离能逐渐减小,O和S元素相比,第一电离能较大的是O,M为Cu元素,Cu2+的核外电子排布式为[Ar]3d9或1s22s22p63s23p63d9;
(2) M为Cu元素,Z为O元素,W为S元素,M2Z为Cu2O,M2W为Cu2S,由于氧离子的半径小于硫离子的半径,则Cu2O比Cu2S的晶格能大,所以Cu2O的熔点比Cu2S的高;
(3) W为S元素,Z为O元素,WZ2为SO2,中心原子S价层电子对数=2+![]() =3,S原子采取sp2杂化,VSEPR模型名称为平面三角形;SO3气态为单分子,该分子中S原子的价层电子对数=3+
=3,S原子采取sp2杂化,VSEPR模型名称为平面三角形;SO3气态为单分子,该分子中S原子的价层电子对数=3+![]() =3,杂化轨道类型为sp2;单键都为σ键,SO3的三聚体环状结构如图(a)所示,该结构的分子中含有12个σ键,SO3由4个原子构成,价电子总数为24,与SO3互为等电子体的分子的化学式为BF3;
=3,杂化轨道类型为sp2;单键都为σ键,SO3的三聚体环状结构如图(a)所示,该结构的分子中含有12个σ键,SO3由4个原子构成,价电子总数为24,与SO3互为等电子体的分子的化学式为BF3;
(4)MRW2为CuFeS2,晶胞中每个Cu原子与4个S原子相连,CuFeS2的晶胞中S原子个数=8、Fe原子个数=4×![]() +4×
+4×![]() +2×
+2×![]() =4、Cu原子个数=8×
=4、Cu原子个数=8×![]() +4×
+4×![]() +1=4,晶胞体积=a2c=(0.524×10-7×0.524×10-7×1.032×10-7)cm3,晶体密度ρ=
+1=4,晶胞体积=a2c=(0.524×10-7×0.524×10-7×1.032×10-7)cm3,晶体密度ρ=![]() =
=![]() =
=![]() g/cm3=
g/cm3=![]() g/cm3。
g/cm3。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案