题目内容
6.下列叙述正确的是( )| A. | 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 | |
| B. |  的消去产物有两种 的消去产物有两种 | |
| C. | 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2═CH-COOCH3 | |
| D. | 可用溴水鉴别乙醛、四氯化碳、苯和乙酸 |
分析 A.甲苯不能使溴的四氯化碳溶液褪色;
B.结构对称,消去产物只有一种;
C.有机物A(C4H6O2)能发生加聚反应,说明含有C=C,可能为酯或酸;
D.乙醛与溴水反应褪色,四氯化碳不溶于水在下层,苯不溶于水,在上层,乙酸与溴水互溶.
解答 解:A.甲苯不能使溴的四氯化碳溶液褪色,可与酸性高锰酸钾发生氧化还原而使高锰酸钾褪色,故A错误;
B.结构对称,消去产物只有一种,为 ,故B错误;
,故B错误;
C.有机物A(C4H6O2)能发生加聚反应,说明含有C=C,可能为酯或酸,为CH2=CHCH2COOH、CH3CH=CHCOOH或CH2=CH-COOCH3,故C错误;
D.乙醛与溴水反应褪色,四氯化碳不溶于水在下层,苯不溶于水,在上层,乙酸与溴水互溶,四者现象不同,可鉴别,故D正确.
故选D.
点评 本题考查有机物的结构和性质,题目难度不大,注意相关知识的把握,易错点为C,注意同分异构体的判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0L1.0mol•L-1的NaClO水溶液中含有的氧原子数为NA | |
| B. | 总质量为ag的CO和N2的混合物中所含原子总数为$\frac{a{N}_{A}}{14}$ | |
| C. | 2.24L 的2H35Cl分子中的中子数是1.9NA | |
| D. | 某密闭容器中盛有0.1mol N2和0.3molH2,在一定条件下充分反应,形成N-H键的数目为0.6NA |
14.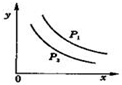 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )| A. | 上述正反应是放热反应 | B. | 上述正反应是吸热反应 | ||
| C. | 增大L的量,平衡正向移动 | D. | a<b |
11.水凝结成冰的过程的焓变和熵变正确的是( )
| A. | △H>0,△S<0 | B. | △H<0,△S>0 | C. | △H>0,△S>0 | D. | △H<0,△S<0 |
15.用1L 1.0mol•L-1NaOH溶液吸收0.8molSO2,所得溶液中的SO32-和HSO3-的物质的量浓度之比是( )
| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
16.同周期元素X、Y可组成化学式为XY2的共价化合物,则X、Y的原子序数可能是( )
| A. | 11和16 | B. | 6和8 | C. | 12和17 | D. | 7和8 |

 .
. ,其名称为2,3-二甲基-2-丁烯.
,其名称为2,3-二甲基-2-丁烯. .
.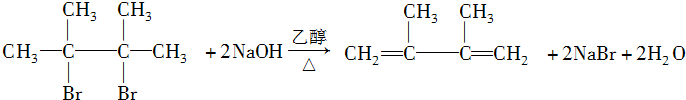 ;写出由E→F2的化学方程式:
;写出由E→F2的化学方程式: .
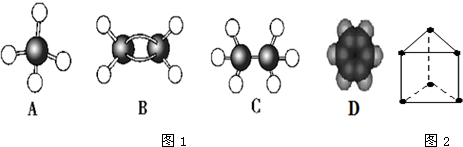
.
 .
.