题目内容
18.现有A、B、C、D四种烃,其球棍模型或比例模型如图1: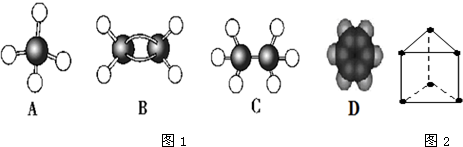
(1)等质量的以上物质完全燃烧时耗去O2的量最多的是CH4(填分子式);
(2)可以用来鉴别A和B的试剂是CD
A、水 B、稀硫酸 C、溴的四氯化碳溶液 D、酸性高锰酸钾溶液
(3)上述四种物质互为同系物的是AC.(填字母)
(4)在一定条件下,B能发生聚合反应,写出该反应的方程式
 .
.(5)物质A可以用于燃料电池,实现了化学能转化为电能;该燃料电池以KOH溶液为电解质溶液,则电池反应的负极反应CH4-8e-+10OH-=CO32-+H2O,电池工作一段时间后,电解质溶液中KOH的物质的量减少.(填增多、减少或不变)
(6)上述四种物质中有一种可以在一定条件下与浓硝酸反应,请写出反应的化学方程式,并注明反应条件.

(7)E是一种新合成的烃,其碳架呈三棱柱体(如图2所示);
①上述物质中与E互为同分异构体的是C6H6.(填分子式)
②E的一氯取代物有1种.
分析 由A、B、C、D四种烃的球棍模型或比例模型可知,A为CH4,B为C2H4,C为C2H6,D为C6H6,
(1)等质量的烃CxHy完全燃烧时,氢元素的质量分数越大,耗氧量越大;
(2)B中含双键,能发生加成、氧化反应;
(3)A、C的结构相似,组成相差1个CH2原子团;
(4)B中含双键,可发生加聚反应;
(5)甲烷在负极上失去电子生成碳酸根离子;电池干燥时消耗KOH;
(6)苯与浓硝酸发生硝化反应生成硝基苯;
(7)由图可知,E中含6个CH,只有一种H.
解答 解:由A、B、C、D四种烃的球棍模型或比例模型可知,A为CH4,B为C2H4,C为C2H6,D为C6H6,
(1)等质量的烃CxHy完全燃烧时,氢元素的质量分数越大,耗氧量越大,CH4、C2H4、C2H6、C6H6中的$\frac{y}{x}$依次为4、2、3、1,故CH4耗O2最多,故答案为:CH4;
(2)B中含双键,与溴发生加成反应、能被高锰酸钾氧化,可鉴别,故答案为:C D;
(3)A、C的结构相似,组成相差1个CH2原子团,二者互为同系物,故答案为:A C;
(4)在一定条件下,B能发生聚合反应,该反应的方程式为 ,
,
故答案为: ;
;
(5)甲烷在负极上失去电子生成碳酸根离子,负极反应为CH4-8e-+10OH-=CO32-+H2O;电池干燥时消耗KOH,则KOH的物质的量减少,
故答案为:CH4-8e-+10OH-=CO32-+H2O;减少;
(6)苯与浓硝酸发生硝化反应生成硝基苯,反应为 ,
,
故答案为: ;
;
(7)由图可知,E中含6个CH,只有一种H,分子式为C6H6,E的一氯取代物有1种,故答案为:C6H6;1.
点评 本题考查较为综合,侧重于有机物的结构和性质的考查,为高考常见题型,难度不大,注意把握有机物的官能团的性质,结合题给信息判断有机物的结构简式.

| A. | 阿司匹林属于解热镇痛药 | |
| B. | 青霉素有青霉素F、G、X、K、V | |
| C. | 胃舒平、苏打片均属于抗酸药 | |
| D. | 青霉素在体内水解可得到一类碱性物质 |
| A. | 把2 mol/L盐酸换成2 mol/L H2SO4 | B. | 碾碎碳酸钙 | ||
| C. | 适当加热 | D. | 增大盐酸的浓度 |
| A. | 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 | |
| B. |  的消去产物有两种 的消去产物有两种 | |
| C. | 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2═CH-COOCH3 | |
| D. | 可用溴水鉴别乙醛、四氯化碳、苯和乙酸 |
| A. | 乙烷 | B. | 乙醇 | C. | 丙烯(CH3CH=CH2) | D. | 苯 |
①NaHCO3②Al ③NH4HCO3④Al(OH)3⑤NaHSO4 ⑥Si.
| A. | ①②③④ | B. | ②③⑤⑥ | C. | ②③⑤ | D. | ②③④⑤⑥ |
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | I | G | ||||
| 3 | B | C | F | H |
(2)A元素与 I元素形成的化合物的化学式是H2O、H2O2,它们都是共价化合物 (填“共价化合物”或“离子化合物”).
(3)在B、C、F中,原子半径最小的是P;
(4)D、E两元素的最高价氧化物的水化物中,酸性较强的是HNO3;
(5)E为气态氢化物为NH3,实验室制取它的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(6)用电子式表示B和H组成化合物的形成过程
 .
. 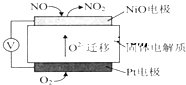 NOx是汽车尾气中的主要污染物之一.
NOx是汽车尾气中的主要污染物之一.