题目内容
14.将8g碳单质在足量氧气中燃烧所得气体通入1L 1mol/L的氢氧化钠溶液中完全吸收后,溶液中物质及物质的量为Na2CO3和NaHCO3、$\frac{1}{3}$mol和$\frac{1}{3}$mol.分析 0.667g碳燃烧生成0.667molCO2,与1molNaOH反应生成Na2CO3和NaHCO3的混合物,由此分析解答.
解答 解:设Na2CO3和NaHCO3的物质的量分别为xmol和ymol,则$\left\{\begin{array}{l}{x+y=\frac{8}{12}}\\{2x+y=1}\end{array}\right.$,解之得:$\left\{\begin{array}{l}{x=\frac{1}{3}}\\{y=\frac{1}{3}}\end{array}\right.$,故答案为:Na2CO3和NaHCO3、$\frac{1}{3}$mol和$\frac{1}{3}$mol.
点评 本题考查了根据反应方程式进行相关物质的计算,根据方程式中各个物理量的关系式进行计算,题目难度中等.

练习册系列答案
相关题目
2.如图所示信息判断,下列离子能够大量共存的一组是( )
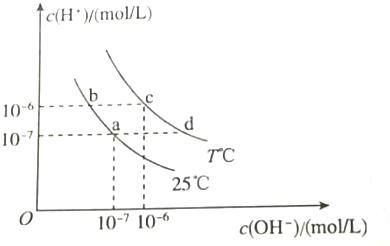

| A. | a点对应的溶液中:Al3+、Na+、Cl-、CO32- | |
| B. | b点对应的溶液中:K+、Ba2+、NO3-、AlO2- | |
| C. | c点对应的溶液中:Fe3+、Na+、I-、SO42- | |
| D. | d点对应的溶液中:Na+、K+、SO32-、Cl- |
19.氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂.下列关于氯化亚砜分子的几何构型和中心原子(S)采取杂化方式的说法正确的是( )
| A. | 三角锥形、sp3 | B. | V形、sp2 | C. | 平面三角形、sp2 | D. | 三角锥形、sp2 |
10.共价键是有饱和性和方向性的,下列有关叙述不正确的是( )
| A. | 共价键的饱和性是由成键原子的未成对电子数决定的 | |
| B. | 共价键的方向性是由成键原子的轨道的方向性决定的 | |
| C. | 共价键的饱和性决定了分子内部的原子的数量关系 | |
| D. | 共价键的饱和性与原子轨道的重叠程度有关 |
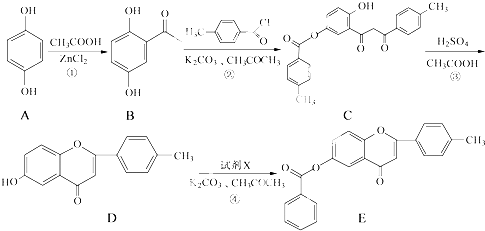
 .
.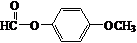 .
.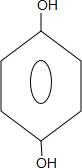 +CH3COOH$\stackrel{ZnCl_{2}}{→}$
+CH3COOH$\stackrel{ZnCl_{2}}{→}$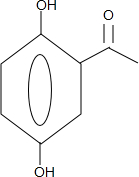 +H2O.
+H2O. .
.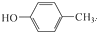 和CH3COOH为原料制备
和CH3COOH为原料制备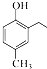 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: