题目内容
【题目】如图所示是酸雨的形成示意图。根据图示回答下列问题。
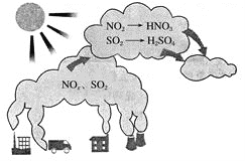
(1)下列气体容易形成酸雨的是_____。
A.CO2 B.SO2 C.N2 D.NO2
(2)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
测试时间/h | 0 | 1 | 2 | 3 | 4 |
与水的pH | 4.73 | 4.63 | 4.56 | 4.55 | 4.55 |
分析数据,回答下列问题:
①雨水样品的pH变化的原因是____(用化学方程式表示)。
②如果将刚取样的上述雨水和自来水相混合,pH将变____,原因是_____(用化学方程式表示)。
(3)下列措施中,可减少酸雨产生的途径的是____(填字母)。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
【答案】BD SO2+H2O![]() H2SO3、2H2SO3+O2=2H2SO4 变小 Cl2+2H2O+SO2=H2SO4+2HCl(或H2SO3+Cl2+H2O=H2SO4+2HCl) C
H2SO3、2H2SO3+O2=2H2SO4 变小 Cl2+2H2O+SO2=H2SO4+2HCl(或H2SO3+Cl2+H2O=H2SO4+2HCl) C
【解析】
(1)酸雨是指pH小于5.6的雨水,酸雨分为硫酸型酸雨和硝酸型酸雨,分别是由SO2和NOx引起,而N2和CO2是空气组成成分,不能引起酸雨,故选项BD正确;答案选BD;
(2)①空气中SO2与水生成H2SO3,NOx的氧化物与水生成HNO3,酸雨放置一段时间后,H2SO3被空气中的氧气氧化成H2SO4,酸性增强,其反应方程式为SO2+H2O![]() H2SO3、2H2SO3+O2=2H2SO4;
H2SO3、2H2SO3+O2=2H2SO4;
②自来水常用Cl2消毒,用上述雨水与自来水混合,SO2与Cl2反应:Cl2+2H2O+SO2=H2SO4+2HCl或H2SO3+Cl2+H2O=H2SO4+2HCl,因此溶液的pH将变小;
(3)①要减少酸雨的产生,需减少SO2的排放,大气中SO2来源主要是化石燃料的燃烧以及含硫矿石的冶炼和硫酸、造纸等生产过程中产生的尾气,煤中含有硫,燃烧过程中生成大量SO2,因此少用煤作燃料或对燃料进行脱硫处理,是减少酸雨的有效措施,故①符合题意;
②把烟囱造高,不能减少酸雨的生成,故②不符合题意;
③燃料脱硫,是减少酸雨的有效措施,故③符合题意;
④在已酸化的土壤中加石灰是为了中和酸,不是为了减少酸雨,故④不符合题意;
⑤开发新能源能从根本上杜绝SO2的产生,故⑤符合题意;
综上所述选项C正确;答案选C。

 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案