题目内容
18.当有机化合物分子中的一个碳原子所连的四个原子或原子团均不相同时,此碳原子就是“手性碳原子”,具有手性碳原子的物质往往具有旋光性,存在对映异构体,如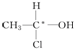 等,下列化合物中存在对映异构体的是( )
等,下列化合物中存在对映异构体的是( )| A. | 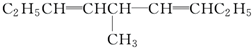 | B. | 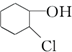 | ||
| C. | 甲酸 | D. | C6H5CH2OCH3 |
分析 根据题意知,手性碳原子必须连接4个不同的原子或原子团,具有手性碳原子的物质往往具有旋光性,存在对映异构体;通过判断有机物分子中是否存在手性碳原子即可得出答案.
解答 解:A.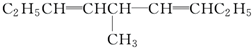 分子中,3个甲基上的碳原子所连接的四个基团有3个是一样的H,2个次甲基上的碳原子所连接的四个基团2个是一样的H,没有手性碳原子,不存在对映异构体,故A错误;
分子中,3个甲基上的碳原子所连接的四个基团有3个是一样的H,2个次甲基上的碳原子所连接的四个基团2个是一样的H,没有手性碳原子,不存在对映异构体,故A错误;
B. 分子中,和羟基相连碳及和氯原子相连碳上连着四个不同的基团,属于手性碳原子,存在对映异构体,故B正确;
分子中,和羟基相连碳及和氯原子相连碳上连着四个不同的基团,属于手性碳原子,存在对映异构体,故B正确;
C.甲酸的结构简式为HCOOH,所以甲酸分子中没有手性碳原子,不存在对映异构体,故C错误;
D.C6H5CH2OCH3中,没有手性碳原子,不存在对映异构,故D错误;
故选B.
点评 本题考查手性碳原子的判断,题目难度不大,正确判断有机物分子中是否含有手性碳原子为解答关键,明确存在手性碳原子条件:手性碳原子一定是饱和碳原子、手性碳原子所连接的四个基团要是不同的.

练习册系列答案
相关题目
13.中小学生使用的涂改液被称为“隐形杀手”,是因为涂改液里主要含有二甲苯 等有机烃类物质,长期接触二甲苯会对血液循环系统产生损害,可导致再生障碍性贫血和骨髓综合症(白血病的前期).下列说法不正确的是( )
| A. | 二甲苯有三种同分异构体 | |
| B. | 二甲苯和甲苯是同系物 | |
| C. | 二甲苯分子中,所有碳原子都在同一个平面上 | |
| D. | 1mol二甲苯完全燃烧后,生成的二氧化碳和水的物质的量相等 |
10.化学与生活密切相关,下列说法正确的是( )
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 地沟油的主要成分是油脂,其组成与汽油、煤油相同 | |
| C. | 合成纤维、人造纤维及光导纤维都属于有机高分子材料 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
7.国际理论与应用化学联合会(IUPAC)在2012年5月30日宣布第116号元素的元素符号是Lv,此前暂用名为Uuh.下列有关叙述中错误的是( )
| A. | Lv位于周期表中第七周期第ⅥA族 | B. | Lv原子的次外层电子数为18 | ||
| C. | Lv为非金属元素 | D. | Lv为放射性元素 |

 -CH3(g)+11H2△H=kJ•mol-1.
-CH3(g)+11H2△H=kJ•mol-1.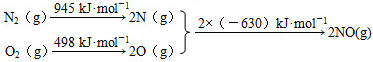 N2(g)+O2(g)=2NO(g)△H=+184kJ•mol-1.
N2(g)+O2(g)=2NO(g)△H=+184kJ•mol-1.