题目内容
15.某学生实验兴趣小组拟用图1装置来完成“NaHCO3和NaCl混合物中NaHCO3含量的测定”的实验.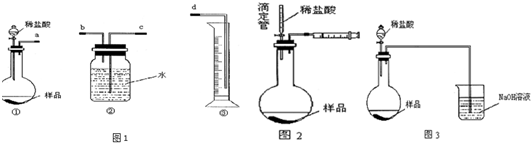
(1)各仪器接口连接顺序是a、b、c、d(用接口字母填写).
(2)该装置连接好而未装药品前,检验气密性的操作是在②中加水浸没长导管,关闭分液漏斗活塞,用手握住圆底烧瓶(或酒精灯微热),若②中长导管内液面上升,则说明气密性好;或在③中加水浸没导管,关闭分液漏斗活塞,用酒精灯微热,若③中导管口产生均匀的气泡,停止加热后,导管末端形成一段水柱且保持一段时间不下降,则说明气密性好.
(3)甲同学认为上述方法误差较大,提出如下改进措施,你认为可行的有BD.(填序号)
A.在滴入盐酸之前,应排净装置内的CO2气体
B.在装置①中稀盐酸换成稀硫酸,装置②中水换成饱和NaHCO3溶液
C.在装置②中水换成饱和Na2CO3溶液
D.滴加盐酸不宜过快
(4)乙同学认为在装置②③之间的导管内会积存水,使测定结果不准,从而改用图2装置.假定滴定管起始读数为V1mL,终了读数为V2mL,而注射器测定排出的气体为V3mL(标准状况下),混合物样品质量为m g,则原混合物中NaHCO3的质量分数的表达式为$\frac{84({V}_{3}+{V}_{1}-{V}_{2})}{22400m}×100%$.(用含V1、V2、V3、m的式子表示).
(5)丙同学改用图3装置,通过测定烧杯的质量.你认为乙、丙两同学的方案中,谁的方案更合理乙同学,理由是:丙同学的方案中,生成的CO2没有全被NaOH溶液吸收.
分析 (1)NaHCO3和NaCl混合物中NaHCO3含量的测定,利用的原理是加入只组成盐酸反应用排水量气法测定生成二氧化碳的体积,进行计算碳酸氢钠含量,量气装置导气管短进长出;
(2)连接装置关闭活塞,末端导气管浸入水中使装置密闭,微热改变装置烧瓶内的压强,观察导气管末端是否有气泡冒出且停止受热,导气管中有一段水柱上升说明装置气密性好;
(3)A、测定气体体积是利用排出液体的液面差和气体含有杂质无关;
B、在装置①中稀盐酸换成稀硫酸,减少氯化氢挥发,装置②中水换成饱和NaHCO3溶液减少二氧化碳的溶解;
C、饱和Na2CO3溶液会和二氧化碳反应生成碳酸氢钠;
D、滴加盐酸过快CO2,CO2不能完全被吸收,排出装置C;
(4)找出二氧化碳的体积,根据碳守恒计算出碳酸氢钠的物质的量,根据m=nM计算碳酸氢钠的质量,即可求出碳酸氢钠的质量分数;
(5)丙同学的方案中,生成的CO2不能全被NaOH溶液吸收.
解答 解:(1)NaHCO3和NaCl混合物中NaHCO3含量的测定,利用的原理是加入盐酸反应用排水量气法测定生成二氧化碳的体积,进行计算碳酸氢钠含生成量,量气装置导气管短进长出,连接顺序为:a、b、c、d,
故答案为:a、b、c、d;
(2)连接装置关闭活塞,末端导气管浸入水中使装置密闭,微热改变装置烧瓶内的压强,观察导气管末端是否有气泡冒出且停止受热,导气管中有一段水柱上升说明装置气密性好,具体步骤为:在②中加水浸没长导管,关闭分液漏斗活塞,用手握住圆底烧瓶(或酒精灯微热),若②中长导管内液面上升,则说明气密性好;或在③中加水浸没导管,关闭分液漏斗活塞,用酒精灯微热,若③中导管口产生均匀的气泡,停止加热后,导管末端形成一段水柱且保持一段时间不下降,则说明气密性好,
故答案为:在②中加水浸没长导管,关闭分液漏斗活塞,用手握住圆底烧瓶(或酒精灯微热),若②中长导管内液面上升,则说明气密性好;或在③中加水浸没导管,关闭分液漏斗活塞,用酒精灯微热,若③中导管口产生均匀的气泡,停止加热后,导管末端形成一段水柱且保持一段时间不下降,则说明气密性好;
(3)A、测定气体体积是利用排出液体的液面差和气体含有杂质无关,故A错误;
B、在装置①中稀盐酸换成稀硫酸,减少氯化氢挥发,装置②中水换成饱和NaHCO3溶液减少二氧化碳的溶解,减少误差,故B正确;
C、饱和Na2CO3溶液会和二氧化碳反应生成碳酸氢钠,使测定二氧化碳体积减少,故C错误;
D、滴加盐酸过快CO2,CO2不能完全被吸收,排出装置C,滴加盐酸不宜过快,故D正确;
故答案为:BD;
(4)盐酸排出的空气的体积是(V2-V1)mL,产生的二氧化碳的体积是V3-(V2-V1),根据碳原子守恒,碳酸氢钠的物质的量是:$\frac{{V}_{3}-({V}_{2}-{V}_{1})}{22400}$mol,原样品中碳酸氢钠的质量分数为:$\frac{\frac{{V}_{3}-({V}_{2}-{V}_{1})}{22400}×84}{m}$×100%=$\frac{84({V}_{3}+{V}_{1}-{V}_{2})}{22400m}×100%$,
故答案为:$\frac{84({V}_{3}+{V}_{1}-{V}_{2})}{22400m}×100%$;
(5)丙同学的方案中,生成的CO2没有全被NaOH溶液吸收,所以方案更合理得为乙,
故答案为:乙同学;丙同学的方案中,生成的CO2没有全被NaOH溶液吸收.
点评 本题考查了物质组成的探究和实验设计方法分析判断,主要是气体体积测定和计算分析,掌握基础是关键,题目难度中等.

| A. | Mn | B. | V | C. | Cr | D. | Cu |
| A. | 正常的人体血液 | B. | 食盐溶液 | C. | 橙汁 | D. | 胃液 |
| X | ||
| Y | ||
| Z |
(1)x元素的单质分子式是He,单质是原子晶体.
(2)自然界中存在一种仅含钙与Y两种元素的天然矿物,其电子式为
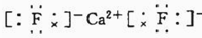 ,属于离子晶体.
,属于离子晶体.(3)Z的氢化物和Y的氢化物沸点高低顺序是:HF>H2S,理由:HF分子之间除了存在分子间作用力,还存在氢键.
(4)X、Y、Z三种元素中,电负性最大的是:F.
| A. | $\frac{1}{5}$mol | B. | $\frac{2}{5}$ mol | C. | $\frac{3}{5}$mol | D. | $\frac{11}{5}$ mol |
| A. | 上述溶液能使甲基橙试剂变黄色 | |
| B. | 室温下,NH3•H2O是比HCN更弱的电解质 | |
| C. | 上述溶液中CN-的水解程度大于NH4+的水解程度 | |
| D. | 室温下,0.1mol/LNaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度 |
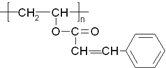 光刻胶是大规模集成电路印刷电路版技术中的关键材料,某一光刻胶的主要成分如图所示,下列有关说法正确的是( )
光刻胶是大规模集成电路印刷电路版技术中的关键材料,某一光刻胶的主要成分如图所示,下列有关说法正确的是( )| A. | 合成此高聚物的单体的化学式为C11H10O2 | |
| B. | 发生加成反应时1 mol该物质可消耗4molH2 | |
| C. | 该物质可稳定存在于碱性溶液中 | |
| D. | 该物质可经过缩聚反应制得 |
 (1)在室温下测得0.1mol•L-1氨水PH=11,则该温度下氨水的电离度α=1.0%
(1)在室温下测得0.1mol•L-1氨水PH=11,则该温度下氨水的电离度α=1.0%