��Ŀ����
����Ŀ����1�����������ʢ�Cu ��Һ�� ��CH3COOH ��NaHCO3 ��H2O ������NaCl ��NH3��H2O ��NH4Cl ����������ʵ��� ������ţ���
��ѧʽ | NH3��H2O | HCN | CH3COOH | H2CO3 |
����ƽ�ⳣ����25�棩 | Kb=1.77��10��5 | Ka=4.93��10��10 | Ka=1.76��10��9 | Ka1=4.30��10��7 Ka2=5.61��10��11 |
��2������ƽ�ⳣ���Ǻ���������ʵ���̶�ǿ���������ϱ��и�������������ʵĵ���ƽ�ⳣ�������п����жϣ�����ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ��������ɴ�С��˳��Ϊ ��
��3������ˮ��̶ȵ�ǿ��ͬ����������ʵĵ���̶���һ����ϵ����ϱ������ݻش��������⣺
��25��ʱ���е�Ũ�ȵ�a��NaCN��Һ b��Na2CO3��Һ c��CH3COONa��Һ��������Һ��pH�ɴ�С��˳��Ϊ ��������Һǰ��ţ�
��Ũ����ͬ��NaCN��Һ��CH3COOK��Һ��ȣ�c(Na+)��c(CN��) c(K+)��c(CH3COO��)����������������������=����
��������������ʵ���Ũ�ȵ�����Ͱ�ˮ��Ϻ���Һ�� �ԣ����������������������������������ӷ���ʽ��ʾԭ�� ��
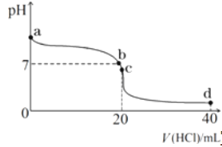
�������£�����0.1mol��L��1�������20ml0.1mol��L��1��ˮ�У���ҺpH�������������ı仯��������ͼ��ʾ��b����ʾ��Һ�е������� ��
��NH4HCO3��Һ�� �ԣ�����������������������������
��4����ϱ������ݣ���NaCN��Һ��ͨ������CO2����������Ӧ�Ļ�ѧ����ʽ ��
���𰸡���1���ۢݢ���2��CH3COOH��H2CO3��HCN
��3����b��a��c �ڣ� ���� NH4++H2O![]() NH3��H2O+H+ ��NH3��H2O NH4Cl�ݼ�
NH3��H2O+H+ ��NH3��H2O NH4Cl�ݼ�
��4��NaCN+H2O+CO2=HCN+NaHCO3
��������
�����������Cu�ǽ������ʲ��ǵ���ʣ���Һ�����ڷǵ���ʣ���CH3COOH����������Һ�в��ֵ��룬����������ʣ���NaHCO3��������ǿ����ʣ���H2O�ܲ��ֵ���������Ӻ����������ӣ�����������ʣ�������NaCl����ȫ���룬����ǿ����ʣ���NH3H2O����Һ�в��ֵ��룬����������ʣ���NH4Cl���Σ�����Һ����ȫ���룬����ǿ����ʣ���������������ʵ����ۢݢ���
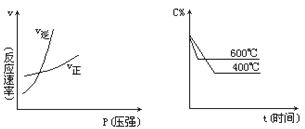
��2������ƽ�ⳣ��Խ��Խ���룬��Һ������Ũ��Խ������Խǿ��������ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ��������ɴ�С��˳��ΪCH3COOH��H2CO3��HCN��
��3������ĵ���ƽ�ⳣ��Խ��Խ���룬����Խǿ�����ε�ˮ��̶�ԽС��25��ʱ���е�Ũ�ȵ�a��NaCN��Һ��b��Na2CO3��Һ��c��CH3COONa��Һ����ˮ��̶ȣ�b��a��c��ˮ��̶�Խ����Һ�ļ���Խǿ����pHԽ����pH��b��a��c��
��Ũ����ͬ��NaCN��Һ��CH3COOK��Һ�У��ֱ���ڵ���غ�Ϊ��c��Na+��+c��H+��=c��CN-��+c��OH-����c��Na+��+c��H+��=c��CH3COO-��+c��OH-������c��Na+��-c��CN-��=c��OH-��-c��H+����c��K+��-c��CH3COO-��=c��OH-��-c��H+����NaCN����Һˮ��̶ȱ�CH3COOK����NaCN��c��OH-��������c��Na+��-c��CN-����c��K+��-c��CH3COO-����
��������������ʵ���Ũ�ȵ�����Ͱ�ˮ��Ϻ������Ȼ�泥��Ȼ������Һ��ˮ�������ԣ���ˮ������ӷ���ʽΪNH4++H2O![]() NH3��H2O+H+��
NH3��H2O+H+��
�������£�����0.1mol/L�������20mL 0.1mol/L��ˮ�У���ҺpH�������������ı仯������ͼ��ʾ��b����ʾ��ҺpH=7����֪�Ȼ����Һ�����ԣ�pH=7��˵����ҺΪ�Ȼ���백ˮ�Ļ�������Һ������ΪNH3H2O��NH4Cl��
����֪NH3H2O��Kb=1.77��10-5��H2CO3��Ka1=4.30��10-7��˵��̼��ĵ���̶�С�����γ���ʱHCO3-��ˮ��̶ȴ�����NH4HCO3��Һ�ʼ��ԣ�
��4���ɱ������ݿ�֪�����ԣ�H2CO3��HCN��HCO3-������NaCN��Һ��ͨ������CO2����������Ӧ�Ļ�ѧ����ʽ��NaCN+H2O+CO2=HCN+NaHCO3��