题目内容
11. 过氧化钙(CaO2)是一种白色结晶性粉末,极微溶于水,不溶于醇类、乙醚等.加热至350°C左右开始分解放出氧气,与水缓慢反应中生成H2O2,易与酸反应生成H2O2.过氧化钙可用于改善水质,处理含重金属粒子废水和治理赤潮,也可用于应急供养等,是一种重要化工原料.
过氧化钙(CaO2)是一种白色结晶性粉末,极微溶于水,不溶于醇类、乙醚等.加热至350°C左右开始分解放出氧气,与水缓慢反应中生成H2O2,易与酸反应生成H2O2.过氧化钙可用于改善水质,处理含重金属粒子废水和治理赤潮,也可用于应急供养等,是一种重要化工原料.Ⅰ.CaO2的制备.
原理:CaCl2+H2O2+2NH3•H2O+6H2O=CaO2•8H2O↓+2NH4Cl
实验步骤:
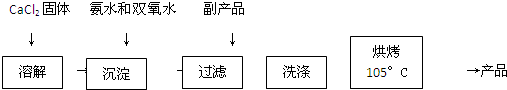
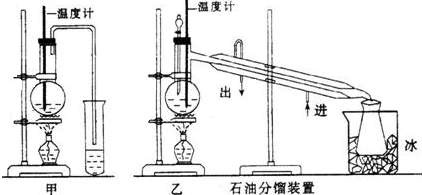
反应装置如图所示:
请回答下面的问题:
(1)a仪器的名称球型冷凝管
(2)加入氨水的作用中和反应生成的HCl,使CaCl2+H2O2?CaO2+2HCl向右进行
(3)沉淀反应时用冰水浴控制温度在0°C左右,其可能的原因是减少双氧水受热分解;降低产物溶解度便于析出(或该反应放热)(写出两种)
(4)过滤后洗涤沉淀的试剂最好用B A.热水 B.冷水 C.乙醇 D.乙醚
Ⅱ.CaO2纯度的测定:将一定量的CaO2溶于稀硫酸,用标准KMnO4溶液滴定生成的H2O2(KMnO4反应后生成Mn2+),计算确定CaO2的含量.
(5)现每次称取0.4000g样品溶解后,用0.1000mol/L的KMnO4溶液滴定,所得的数据如下表所示,则样品的纯度90.00
| 实验序号 | ① | ② | ③ | ④ |
| 消耗 KMnO4体积/mL | 19.98 | 20.02 | 20.20 | 20.00 |
A.烘烤时间不足
B.配制KMnO4标准溶液定容时俯视容量瓶刻度线
C.在洁净干燥的酸式滴定管中未润洗即装标准液
D.滴定前尖嘴部分有气泡,滴定后消失.
分析 CaO2是一种重要化工原料,是一种白色结晶性粉末,极微溶于水,不溶于醇类、乙醚等,加热至350°C左右开始分解放出氧气,与水缓慢反应中生成H2O2,易与酸反应生成H2O2,本题是工业制备CaO2的流程探究与评价,涉及实验操作中冷凝管的识别,加氨水中和酸,促进平衡的移动,降温防过氧化氢的分解等,还考查了利用滴定原理分析样品的纯度及误差分析,据此可作答;
(Ⅰ)(1)根据装置中a的构造可知a为球型冷凝管;
(2)根据可逆反应CaCl2+H2O2?CaO2+2HCl中氯化氢对化学平衡的影响角度分析;
(3)从双氧水的稳定性、该反应的反应热、温度对过氧化钙的溶解度的影响等方面分析;
(4)过氧化钙极微溶于水,反应后产物中杂质不溶于乙醇、乙醚,且在冷水中过氧化钙溶解度小,据此进行解答;
(Ⅱ)(5)先判断滴定数据的有效性,然后计算出消耗高锰酸钾溶液的平均体积,再根据n=cV计算出高锰酸钾的物质的量,然后根据电子守恒计算出每次消耗的过氧化钙的物质的量,根据m=nM计算出样品中过氧化钙的质量,最后计算出过氧化钙的纯度;
(6)A.烘烤时间不足,样品中含有杂质水分,导致纯度降低;
B.在洁净干燥的酸式滴定管中未润洗即装标准液,导致标准液被稀释,滴定过程中消耗的标准液体积偏大;
C.滴定前尖嘴处有气泡,滴定后消失,导致消耗的标准液体积偏大;
D.配制KMnO4标准溶液定容时俯视容量瓶标线,配制的标准液浓度偏高,滴定过程中消耗的标准液体积偏小,测定结果偏低
解答 解:(Ⅰ)(1)图2中仪器a为球型冷凝管,起到冷凝作用,故答案为:球型冷凝管;
(2)氯化钙与双氧水的反应方程式为:CaCl2+H2O2?CaO2+2HCl,加入氨水可以与氯化氢发生中和反应,使该可逆反应向着生成过氧化钙的方向移动,提高的过氧化钙的产率,故答案为:中和反应生成的HCl,使CaCl2+H2O2?CaO2+2HCl向右进行;
(3)由于温度较高时双氧水容易分解,会导致过氧化钙产率下降,且温度降低时过氧化钙的溶解度减小,有利于过氧化钙的析出,所以沉淀反应时常用冰水浴控制温度在0℃左右,
故答案为:减少双氧水受热分解;降低产物溶解度便于析出(或该反应放热);
(4)A.热水:过氧化钙在热水中溶解度较大,降低了过氧化钙的产率,故A错误;
B.冷水:过氧化钙极微溶于水,且杂质都易溶于水,可用冷水洗涤过氧化钙,故B正确;
C.乙醇:过氧化钙不溶于乙醇,但是杂质不溶于乙醇,且提高了成本,故C错误;
D.乙醚:过氧化钙不溶于乙醚,但杂质也不溶于乙醚,且乙醚成本较高,故D错误;
故答案为:B;
(Ⅱ)、(5)根据表中消耗高锰酸钾溶液的体积数据可知,第三次数据与其它三组误差较大,应该舍弃;则滴定中消耗酸性高锰酸钾的平均体积为$\frac{19.98+20.02+20.00}{3}$mL=20.00mL,每次滴定消耗的高锰酸钾的物质的量为:n(KMnO4)=0.1000mol/L×0.02L=0.002mol,
KMnO4反应后生成Mn2+,化合价降低7-2)=5价,CaO2被氧化成氧气,化合价从-1升高到0价,至少升高:[0-(-1)]×2=2,根据化合价升降相等可得反应的关系式:2KMnO4~5CaO2,则每次称取0.4000g样品中含有的过氧化钙的物质的量为:n(CaO2)=$\frac{5}{2}$×n(KMnO4)=0.002mol×$\frac{5}{2}$=0.005mol,
所以该样品中过氧化钙的纯度为$\frac{0.005mol×72g/mol}{0.400g}$×100%=90.00%,
故答案为:90.00%;
(6)A.烘烤时间不足,样品中含有杂质水分,导致样品中过氧化钙的纯度偏小,故A正确;
B.配制KMnO4标准溶液定容时俯视容量瓶标线,导致标准液浓度偏高,滴定过程中营养样品中过氧化钙的物质的量不变,则消耗的标准液体积偏小,测定的过氧化钙的纯度偏小,故B正确;
C.在洁净干燥的酸式滴定管中未润洗即装标准液,不影响标准液的浓度,测定结果无影响,故C错误;
D.滴定前尖嘴处有气泡,滴定后消失,导致消耗的标准液体积偏大,根据关系式计算出的过氧化钙的质量偏大,过氧化钙的纯度偏高,故D错误;
故答案为:AB.
点评 本题考查形式为物质制备流程图题目,涉及中和滴定中的误差分析、物质的检验及化学计算等问题,题目难度较大,做题时注意分析题中关键信息、明确实验基本操作方法,本题较为综合,充分考查了学生的分析、理解能力及化学实验、化学计算能力.

 阅读快车系列答案
阅读快车系列答案| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铝片插入硝酸汞溶液中:Al+Hg2+=Al3++Hg | |
| C. | Ba(OH)2与稀H2SO4反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 盐酸除铁锈:O2-+2H+═H2O |
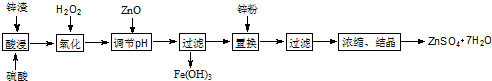
(1)酸浸时温度和时间对锌浸出率的影响如表.
| 酸浸时间/h | 酸浸温度/℃ | 锌浸出率/% |
| 2 | 80 | 87 |
| 2 | 90 | 95 |
| 2 | 110 | 85.3 |
| 3 | 95 | 94.5 |
| 2.5 | 95 | 94 |
 综合考虑,反应的最佳温度和时间是2h、90℃
综合考虑,反应的最佳温度和时间是2h、90℃(2)氧化时也可改通空气,其原因是4Fe2++O2+4H+═4Fe3++2H2O.(用离子方程式表示)
(3)加入锌粉的目的是除去Cu2+.
(4)检验Fe3+是否除尽的方法是取第一次过滤后的滤液少许于试管中,加KSCN溶液,若溶液无血红色出现,则Fe3+已除尽.
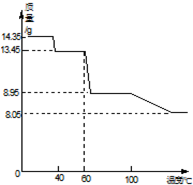
(5)取14.35gZnSO4•7H2O加热分解,加热过程中,固体质量随温度的变化如图所示.写出从60℃到80℃时发生的反应ZnSO4•6H2O$\frac{\underline{\;△\;}}{\;}$ZnSO4•H2O+5H2O.(用化学方程式表示)
 科研生产中常涉及碳的化合物.请回答下列问题:
科研生产中常涉及碳的化合物.请回答下列问题:(1)700℃时,向容积为3L的密闭容器中充人一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见表(表中t2>t1):
| 反应时间/min | N[CO(g)]mol | N[H2O(g)]mol |
| 0 | 1.8 | 0.9 |
| t1 | 1.2 | |
| t2 | y | 0.3 |
②保持其他条件不变,起始时向容器中充入0.9mol CO和1.8mol H2O(g),达平衡时,CO2的物质的量浓度c(CO2)=0.2mol/L.
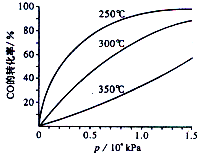
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下平衡转化率与压强的关系如图所示.该反应的△H<0(填“>”、“=”或“<”),实际生产条件控制在250℃,1.3×l04kPa左右,选择此压强的理由是在1.3×l04kPa左右,CO的转化率已经较高,再增大压强,对设备要求较高,增大成本.
(3)CH4和H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g),将等物质的量的CH4和H2O(g)充入2L恒容密闭反应器,某温度下反应达平衡,平衡常数值K=27,此时测得n(CO)=0.2mol,通过计算求CH4的平衡转化率(保留2位小数).
| A. | $\frac{2b-a}{20}$ | B. | 2b-a | C. | 5b-$\frac{5a}{2}$ | D. | 10b-5a |
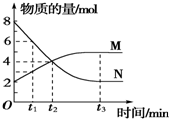 一定温度下,在2L的恒容密闭容器内发生的反应中M、N的物质的量随反应时间变化的曲线如图所示.请回答下列问题:
一定温度下,在2L的恒容密闭容器内发生的反应中M、N的物质的量随反应时间变化的曲线如图所示.请回答下列问题: