题目内容
【题目】已知溶液中的化学反应大多是离子反应。根据要求回答下列问题。
(1)水存在如下平衡:H2O+H2O![]() H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向________(填 “左”或“右”)移动, 且所得溶液显____ 性。
H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向________(填 “左”或“右”)移动, 且所得溶液显____ 性。
(2)向水中加NaHCO3固体,水的电离平衡向____(填“左”或“右”)移动,且所得溶液显____ 性。
(3)常温下,0.1 mol·L-1 CH3COONa溶液的pH为9,则由水电离出的c(H+)=________。
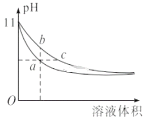
(4)若取pH、体积均相等的NaOH溶液和氨水分别加水稀释m倍、n倍后pH仍相等,则m____n ( 填“>”“<”或“=”)。
【答案】左 酸 右 碱 1×10-5 mol/L <
【解析】
(1)硫酸氢钠完全电离生成氢离子,导致溶液呈强酸性,抑制水电离;
(2)向水中加NaHCO3固体,是强碱弱酸盐,水解对水的电离起促进作用,溶液呈碱性;
(3)能水解的盐溶液促进了水的电离,碱溶液中的氢离子是水电离的,CH3COONa溶液中的氢氧根离子是水电离的;
(4)稀释会促进弱电解质的电离。
(1)硫酸氢钠完全电离生成氢离子,导致溶液呈强酸性,抑制水电离,水的电离平衡逆向移动,因此,本题正确答案是:左;酸;
(2)向水中加NaHCO3固体,是强碱弱酸盐,水解对水的电离起促进作用,所以水的电离平衡向右移动,谁强显谁性,溶液呈碱性,
因此,本题正确答案是:右;碱;
(3)能水解的盐溶液促进了水的电离,碱溶液中的氢离子是水电离的,CH3COONa溶液中的氢氧根离子是水电离的,所以c(OH-)=![]() =1×10-5mol/L,水电离出氢离子与氢氧根离子的浓度相等,
=1×10-5mol/L,水电离出氢离子与氢氧根离子的浓度相等,
因此,本题正确答案是:1×10-5 mol/L;
(4)稀释会促进弱电解质的电离,故若取pH、体积均相等的NaOH和氨水分别加水稀释m倍、n稀释后pH仍相等,则氨水稀释倍数大,
因此,本题正确答案是:<。