题目内容
3.下面关于电解质的叙述中错误的是( )| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | NaHSO4电离时生成的阳离子有氢离子,所以是酸 | |
| D. | 纯水的导电性很差,但水不是电解质 |
分析 A.非电解质在水溶液和熔融状态下都不能导电;
B.无论电解质还是非电解质,都一定为化合物,单质和混合物既不是电解质,也不是非电解质;
C.能电离出的阳离子全部是H+的化合物叫做酸,据此解答;
D.纯水能够电离出氢离子和氢氧根离子,水为电解质.
解答 解:A.在水溶液和熔融状态下都不能导电的化合物为非电解质,故A正确;
B.电解质和非电解质都一定为化合物,单质和混合物不属于电解质和非电解质,故B正确;
C.电离出的阳离子全部是H+的化合物叫做酸,能电离出H+的化合物不一定是酸,硫酸氢钠能电离出氢离子,NaHSO4=Na++H++SO42-,属于盐,故④错误,故C错误;
D.纯水能够电离出氢离子和氢氧根离子,所以水为极弱的电解质,故D错误;
故选CD.
点评 本题考查了电解质与非电解质的概念及判断,题目浓度不大,注意掌握电解质与非电解质的根据及区别,明确电解质、非电解质与溶解度没有必然关系.

练习册系列答案
相关题目
13.铜和浓硫酸反应制取SO2气体并回收硫酸铜的实验,不能达到目的是( )

| A. | 用装置甲制取二氧化硫气体 | |
| B. | 用装置乙收集二氧化硫气体 | |
| C. | 用适量CuO粉末中和反应后溶液,用装置丙过滤 | |
| D. | 用装置丁蒸发浓缩CuSO4溶液 |
14.将过量铁粉放入100mL,2mol/L的HNO3溶液中,充分反应后,若还原产物只有NO,所能溶解的铁的质量为( )
| A. | 2.8g | B. | 4.2g | C. | 5.6 g | D. | 11.2g |
18.将4gNaOH溶于水中,若要使每100个H2O分子中含有1个Na+,则需要水的物质的量是( )
| A. | 10mol | B. | 0.1mol | C. | 1mol | D. | 100mol |
15. 据英国媒体报道,某品牌牙膏中含有的消毒剂三氯生,遇到含氯的自来水时能生成哥罗芳(三氯甲烷),哥罗芳能引发肝病甚至致癌.已知三氯生的结构简式如图所示,下列有关说法不正确的是( )
据英国媒体报道,某品牌牙膏中含有的消毒剂三氯生,遇到含氯的自来水时能生成哥罗芳(三氯甲烷),哥罗芳能引发肝病甚至致癌.已知三氯生的结构简式如图所示,下列有关说法不正确的是( )
 据英国媒体报道,某品牌牙膏中含有的消毒剂三氯生,遇到含氯的自来水时能生成哥罗芳(三氯甲烷),哥罗芳能引发肝病甚至致癌.已知三氯生的结构简式如图所示,下列有关说法不正确的是( )
据英国媒体报道,某品牌牙膏中含有的消毒剂三氯生,遇到含氯的自来水时能生成哥罗芳(三氯甲烷),哥罗芳能引发肝病甚至致癌.已知三氯生的结构简式如图所示,下列有关说法不正确的是( )| A. | 三氯生的分子式:C12H7Cl3O2 | B. | 哥罗芳属于烃类 | ||
| C. | 三氯生属于芳香族化合物 | D. | 哥罗芳不易溶于水 |
13.下列说法正确的是( )
| A. |  表示在其他条件不变时,2SO2 (g)+02 (g)?2S03 (g)转化关系中,纵坐标表示02的转化率 | |
| B. |  表示用0.1mol/L NaOH溶液分别滴定等浓度、等体积的盐酸和醋酸,其中实线为滴定醋酸的曲线 | |
| C. | 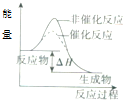 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| D. | 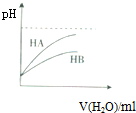 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则酸性HA<HB |
