题目内容
12.1mol O2含有:1.204×1024个氧分子,2.408×1024个氧原子,3.85×1025个电子.分析 氧气是双原子分子,然后以物质的量为中心运用公式,求相关量.
解答 解:1mol O2中含有1mol氧分子,
n(O)=2n(O2)=2×1mol=2mol;
N(O2)=2mol×6.02×1023=1.204×1024,
N(O)=2mol×6.02×1023×2=2.408×1024,
1mol O2含有16个电子,电子数为2.408×1024×16=3.85×1025
故答案为:1.204×1024;2.408×1024;3.85×1025.
点评 本题考考查微粒的物质的数目和物质的量之间的转化关系,难度不大,注意根据化学式确定原子数目与物质的物质的量关系.

练习册系列答案
相关题目
2.只给出下列甲中和乙中对应的量,不能组成一个求物质的量公式的是( )
| 选项 | 甲 | 乙 |
| A | 物质的粒子数 | 阿伏加德罗常数 |
| B | 标况下气体的体积 | 标况下气体摩尔体积 |
| C | 固体的体积 | 固体的密度 |
| D | 溶液的物质的量浓度 | 溶液的体积 |
3.下面关于电解质的叙述中错误的是( )
| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | NaHSO4电离时生成的阳离子有氢离子,所以是酸 | |
| D. | 纯水的导电性很差,但水不是电解质 |
7.某学生用托盘天平称量食盐,将食盐放在右盘,砝码放在左盘,称得食盐的质量为15.5g(1g以下用游码).该学生所称量的食盐的实际质量是( )
| A. | 15.5 g | B. | 15.0 g | C. | 14.5 g | D. | 16.0 g |
4.除去溶液中溶解的杂质,下列做法中不正确的是(括号内的物质为杂质)( )
| A. | NaCl溶液(Na2SO4)加入适量Ba(NO3)2溶液后,过滤 | |
| B. | NaNO3溶液(NaCl)加入适量AgNO3溶液后,过滤 | |
| C. | NaCl溶液(CaCl2)加入适量Na2CO3溶液后,过滤 | |
| D. | NaCl溶液(碘I2)加入四氯化碳后,分液 |
1.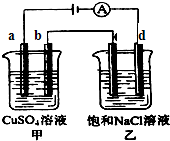 如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
 如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )| A. | 甲烧杯中a极上最多可析出铜0.64g | |
| B. | 甲烧杯中b极上电极反应式4OH--4e-═2H2O+O2↑ | |
| C. | 乙烧杯中滴入酚酞试液,d极附近先变红 | |
| D. | 烧杯中c极上电极反应式为4H++4e-═2H2↑ |
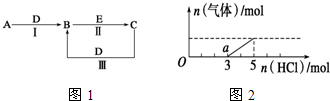
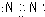 .②写出反应Ⅰ的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
.②写出反应Ⅰ的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.