题目内容
13.铜和浓硫酸反应制取SO2气体并回收硫酸铜的实验,不能达到目的是( )
| A. | 用装置甲制取二氧化硫气体 | |
| B. | 用装置乙收集二氧化硫气体 | |
| C. | 用适量CuO粉末中和反应后溶液,用装置丙过滤 | |
| D. | 用装置丁蒸发浓缩CuSO4溶液 |
分析 A.Cu与浓硫酸反应需要加热;
B.二氧化硫的密度比空气的密度大,且有毒;
C.CuO不溶于水,分离不溶性固体与溶液;
D.蒸发浓缩CuSO4溶液,需要蒸发皿、酒精灯等.
解答 解:A.Cu与浓硫酸反应需要加热,图中缺少酒精灯,不能制取气体,故A错误;
B.二氧化硫的密度比空气的密度大,且有毒,则图中向上排空气法及尾气处理装置均合理,故B正确;
C.CuO不溶于水,分离不溶性固体与溶液,则用装置丙过滤可分离,故C正确;
D.蒸发浓缩CuSO4溶液,需要蒸发皿、酒精灯等,则图中仪器及装置均合理,故D正确;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握气体的制备及收集、混合物分离提纯方法及原理、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
18.下列有关说法正确的是( )
| A. | 铁碳合金发生电化腐蚀时,电子由碳流向铁 | |
| B. | 6NO(g)+4NH3(g)═5N2(g)+6H2O(l)常温下能自发进行,则该反应△H>0 | |
| C. | 常温下,用水稀释0.1mol•L-1NH4Cl溶液,则$\frac{c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})•(O{H}^{-})}$的值不变 | |
| D. | 对于溴乙烷的水解反应(△H>0),加入NaOH 并加热,该反应的反应速率和平衡常数均增大 |
5.下列有关有机物的叙述正确的是( )
| A. | 某烷烃的名称为2,2,4,4-四甲基-3,3,5-三乙基己烷 | |
| B. | 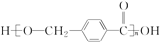 分子中只存在羧基、羟基两种官能团 分子中只存在羧基、羟基两种官能团 | |
| C. | PETG的结构简式为: 合成PETG的单体有4种 合成PETG的单体有4种 | |
| D. | 化合物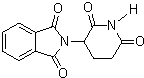 在酸性条件下水解,所得溶液加碱后加热有NH3生成 在酸性条件下水解,所得溶液加碱后加热有NH3生成 |
2.只给出下列甲中和乙中对应的量,不能组成一个求物质的量公式的是( )
| 选项 | 甲 | 乙 |
| A | 物质的粒子数 | 阿伏加德罗常数 |
| B | 标况下气体的体积 | 标况下气体摩尔体积 |
| C | 固体的体积 | 固体的密度 |
| D | 溶液的物质的量浓度 | 溶液的体积 |
3.下面关于电解质的叙述中错误的是( )
| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | NaHSO4电离时生成的阳离子有氢离子,所以是酸 | |
| D. | 纯水的导电性很差,但水不是电解质 |


