题目内容
【题目】由N、F、S、Cl、Cu、Ni等元素组成的物质在生产、生活中有着广泛的用途,回答下列问题.
(1)聚四氟乙烯是一种准晶体,该晶体是一种无平移周期序但有严格准周期位置序的独特晶体.可通过________方法区分晶体、准晶体和非晶体,![]() 四氟乙烯分子中含
四氟乙烯分子中含![]() 键数目为________.
键数目为________.
(2)![]() 原子的价层电子轨道表达式
原子的价层电子轨道表达式![]() 价层电子排布图
价层电子排布图![]() 为________.
为________.
(3)![]() 、Cl、S电负性由大到小的顺序为________.
、Cl、S电负性由大到小的顺序为________.
(4)![]() 氟酸锑
氟酸锑![]() 是一种超强酸,离子
是一种超强酸,离子![]() 的空间构型为________,依次写出一种与
的空间构型为________,依次写出一种与![]() 具有相同空间构型和键合形式的分子和阴离子:________、________.
具有相同空间构型和键合形式的分子和阴离子:________、________.
(5)![]() 氟化铵
氟化铵![]() 可用作玻璃蚀刻剂、防腐剂、消毒剂等.
可用作玻璃蚀刻剂、防腐剂、消毒剂等.![]() 的中心原子的杂化类型是________;氟化铵中存在________
的中心原子的杂化类型是________;氟化铵中存在________![]() 填字母
填字母![]() .
.
A.离子键
B.![]() 键
键
C.![]() 键
键
(6)![]() 的密度为
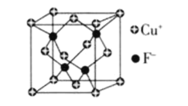
的密度为![]() ,CuF的晶胞结构如下图.CuF的晶胞参数
,CuF的晶胞结构如下图.CuF的晶胞参数![]() ________
________![]() 列出计算式
列出计算式![]() .
.
【答案】![]() 射线衍射
射线衍射 ![]()

![]()
![]() 型
型 ![]() 或
或![]()
![]()
![]()
![]()

【解析】
(1)X射线的衍射可以区分晶体、准晶体和非晶体;1个四氟乙烯分子中含5个![]() 键;
键;
(2)![]() 原子的价层电子排布式是3d84s2;
原子的价层电子排布式是3d84s2;
![]() 同周期自左而右电负性增大、同主族自上而下电负性减小;
同周期自左而右电负性增大、同主族自上而下电负性减小;
(4)离子![]() 中心原子F的价电子对数是
中心原子F的价电子对数是![]() ,孤电子对数是2;
,孤电子对数是2;
(5)![]() 的中心原子N的价电子对数是
的中心原子N的价电子对数是![]() ;
;
(6)根据![]() 晶胞的摩尔质量÷(晶胞的体积×
晶胞的摩尔质量÷(晶胞的体积×![]() )计算晶胞的边长。
)计算晶胞的边长。
![]() 从外观无法区分三者,但通过X射线的衍射实验,三者得到的谱线特征不同,X射线衍射实验可以区分三者;四氟乙烯,其结构简式为
从外观无法区分三者,但通过X射线的衍射实验,三者得到的谱线特征不同,X射线衍射实验可以区分三者;四氟乙烯,其结构简式为![]() ,1mol四氟乙烯分子中含
,1mol四氟乙烯分子中含![]() 键为5mol,则
键为5mol,则![]() 四氟乙烯分子中含
四氟乙烯分子中含![]() 键数目为
键数目为![]() ;
;
![]() 基态Ni原子价层电子的排布式为
基态Ni原子价层电子的排布式为![]() ,由泡利原理、洪特规则,可得轨道表达式为:
,由泡利原理、洪特规则,可得轨道表达式为:![]() ;
;
![]() 同周期自左而右电负性增大、同主族自上而下电负性减小,所以电负性:
同周期自左而右电负性增大、同主族自上而下电负性减小,所以电负性:![]() ;
;
![]() 中心原子F的价电子对数是
中心原子F的价电子对数是![]() ,孤电子对数是2,所以为V形;
,孤电子对数是2,所以为V形;
![]() 的N原子价电子对数是
的N原子价电子对数是![]() ,为
,为![]() 杂化,氟化铵为离子化合物,含有离子键和共价键,即
杂化,氟化铵为离子化合物,含有离子键和共价键,即![]() 键和离子键,没有双键,所以不含
键和离子键,没有双键,所以不含![]() 键;
键;
![]() 的密度为
的密度为![]() ,晶胞中F的个数为4,Cu为
,晶胞中F的个数为4,Cu为![]() ,则
,则 ,
, 。
。

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案