题目内容
10.20℃时,NaCl溶解于水的实验数据如下表所示| 实验序号 | 水的质量/g | 加入的NaCl质量/g | 未溶的NaCl质量/g |
| ① | 10 | 2 | 0 |
| ② | 10 | 3 | 0 |
| ③ | 10 | 4 | 0.4 |
| A. | 实验①所得的溶液为饱和溶液 | |
| B. | 实验②所得的溶液为饱和溶液 | |
| C. | 20℃时NaCl的溶解度为30g | |
| D. | 实验①所得溶液的溶质质量分数为16.7% |
分析 由表中数据可知,随着氯化钠的不断加入,溶液的质量在增加,当10g水中溶解了3.6g氯化钠后不再溶解,说明已经达到饱和状态,说明10g水中最多溶,3.6克氯化钠,溶解度s=$\frac{m(溶质)}{m(溶剂)}$×100%=$\frac{3.6g}{10g}$×100=36g;实验①所得溶液的溶质质量分数=$\frac{m(溶质)}{m(溶液)}$×100%=$\frac{2g}{12g}$×100%=16.7%,据此解答.
解答 解:A.依据图中数据可知,该温度下,10g水中最多溶解3.6g,所以当溶解2g还未达到饱和,故A错误;
B.依据图中数据可知,该温度下,10g水中最多溶解3.6g,所以当溶解2g还未达到饱和,故B错误;
C.由表中数据可知,随着氯化钠的不断加入,溶液的质量在增加,当10g水中溶解了3.6g氯化钠后不再溶解,说明已经达到饱和状态,说明10g水中最多溶,3.6克氯化钠,溶解度s=$\frac{m(溶质)}{m(溶剂)}$×100%=$\frac{3.6g}{10g}$×100=36g,故C错误;
D.实验①所得溶液的溶质质量分数═$\frac{m(溶质)}{m(溶液)}$×100%=$\frac{2g}{12g}$×100%=16.7%,故D正确;
故选:D.
点评 本题考查了饱和溶液的性质及溶液质量分数的判断,明确溶解度的概念是解题关键,题目难度不大.

练习册系列答案
相关题目
20. 将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )
将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )
①试管内黄绿色逐渐消失 ②试管内黄绿色加深
③无任何现象④试管内液面上升⑤试管内壁上有油状物生成.
 将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )
将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )①试管内黄绿色逐渐消失 ②试管内黄绿色加深
③无任何现象④试管内液面上升⑤试管内壁上有油状物生成.
| A. | ① | B. | ①④和⑤ | C. | ①和⑤ | D. | ②和⑤ |
18.下列各醇中,能发生消去反应,且生成的烯烃只有一种的( )
| A. | CH3CH2CH(OH)CH3 | B. | CH3OH | C. | 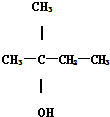 | D. |  |
5.下列有机物的命名正确的是( )
| A. | 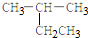 2-乙基乙烷 | B. | 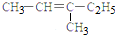 3-甲基-3-戊稀 3-甲基-3-戊稀 | C. | 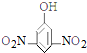 2,4-二硝基苯酚 2,4-二硝基苯酚 | D. |  2,3-丁二醇 |
15.甲烷和乙烯是两种重要的有机物,关于它们的说法不正确的是( )
| A. | 乙烯是重要的化工原料 | |
| B. | 甲烷和乙烯互为同系物 | |
| C. | 甲烷和乙烯可以用溴水加以鉴别 | |
| D. | 甲烷是最简单的有机物,是天然气的主要成分 |
20.钾的金属活动性比钠强,根本原因是( )
| A. | 钾的密度比钠的小 | B. | 加热时,钾比钠更易气化 | ||
| C. | 钾与水反应比钠与水反应更剧烈 | D. | 钾原子的电子层比钠原子多一层 |
 .
.