题目内容
【题目】根据所给的实验装置,下列有关实验的相关叙述正确的是
选项 | 实验装置 | 相关叙述 |
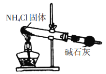
A |
| 实验室可以用该装置和药品制取氨气 |
B |
| 反应过程中,温度降低,Ba(OH)2·8H2O与NH4Cl反应是吸热反应 |
C |
| ①中反应比②中快,说明温度升高可以加快反应速率 |
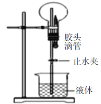
D |
| 只有氨气等极易溶于水的气体才能利用该装置形成喷泉 |
A.AB.BC.CD.D
【答案】B
【解析】
A.实验室制取氨气是加热氯化铵和氢氧化钙固体,图中原料缺少氢氧化钙固体,A错误;
B.温度降低,可知Ba(OH)2·8H2O与NH4Cl反应是吸热反应,B正确;
C.①中滴加了氯化铁溶液作催化剂,不能说明是温度的影响导致反应速率加快的,C错误;
D.喷泉的形成是由于氨气溶于水后,烧瓶内的压强小于大气压,因此只要烧瓶产生较大压强差就能产生喷泉现象,D错误;
答案选B。

 名校课堂系列答案
名校课堂系列答案【题目】下表是A、B、C三种有机物的相关信息:
A | ①能使溴的四氯化碳溶液褪色;②填充模型为: |
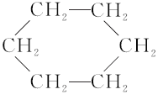
B | ①可以从煤干馏生成的煤焦油中提取;②填充模型为: |
C | 工业生产中可通过A与H2O加成获得;②相对分子质量为46 |
请结合上述信息,回答下列问题:
(1)有机物A的结构式为___________
(2)B与浓硝酸在一定条件下发生反应的化学方程式为__________
(3)有机物C的结构简式为__________。
(4)①C与乙酸反应的化学方程式为____________
②C在铜催化和加热条件下,与O2反应的化学方程式为___________。
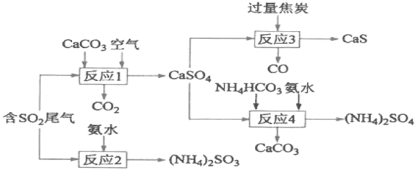
【题目】硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:

(1)仪器a的名称是_______,仪器b的名称是_______。b中利用质量分数为70%80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______。c中试剂为_______
(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-Fe(S2O3)33-(紫黑色)
装置 | 试剂X | 实验现象 |
| Fe2(SO4)3溶液 | 混合后溶液先变成紫黑色,30s后几乎变为无色 |
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______(填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294gmol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______molL-1