题目内容
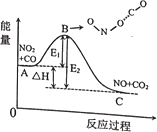
【题目】下表是A、B、C三种有机物的相关信息:
A | ①能使溴的四氯化碳溶液褪色;②填充模型为: |
B | ①可以从煤干馏生成的煤焦油中提取;②填充模型为: |
C | 工业生产中可通过A与H2O加成获得;②相对分子质量为46 |
请结合上述信息,回答下列问题:
(1)有机物A的结构式为___________
(2)B与浓硝酸在一定条件下发生反应的化学方程式为__________
(3)有机物C的结构简式为__________。
(4)①C与乙酸反应的化学方程式为____________
②C在铜催化和加热条件下,与O2反应的化学方程式为___________。
【答案】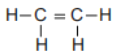
![]() +HO-NO2
+HO-NO2![]()
![]() +H2O C2H5OH CH3COOH +HOCH2CH3
+H2O C2H5OH CH3COOH +HOCH2CH3![]() CH3COOCH2CH3+ H2O 2CH3CH2OH + O2
CH3COOCH2CH3+ H2O 2CH3CH2OH + O2![]() 2CH3CHO + 2H2O
2CH3CHO + 2H2O
【解析】
A能使溴的四氯化碳溶液褪色,结合其填充模型可知应含有碳碳双键,A为CH2=CH2;B可以可以从煤干馏生成的煤焦油中提取,结合其填充模型可知为苯;C可通过A与H2O加成获得,相对分子质量为46,所以C为CH3CH2OH。
(1)A为乙烯,其结构式为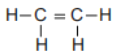 ;
;
(2)苯与浓硝酸在浓硫酸、加热(50℃~60℃)的条件下发生取代反应生成硝基苯和水,化学方程式为![]() +HO-NO2
+HO-NO2![]()
![]() +H2O;
+H2O;
(3)C为乙醇,结构简式为C2H5OH;
(4)①乙醇和乙酸在浓硫酸加热的条件下可以发生酯化反应生成乙酸乙酯,化学方程式为CH3COOH +HOCH2CH3![]() CH3COOCH2CH3+ H2O;
CH3COOCH2CH3+ H2O;
②C在铜催化和加热条件下被氧气氧化成乙醛,化学方程式为2CH3CH2OH + O2![]() 2CH3CHO + 2H2O。
2CH3CHO + 2H2O。

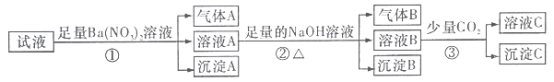
【题目】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
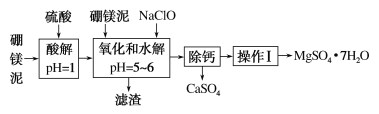
根据题意回答下列问题:
(1)实验中需用1 mol·L-1的硫酸800 mL,若用18.4 mol·L-1的浓硫酸来配制,量取浓硫酸时,需使用的量筒的规格为________。
A 10 mL B 20 mL C 50 mL D 100 mL
(2)加入的NaClO可将Mn2+氧化为MnO2,反应的离子方程式为:___________________,还有一种离子也会被NaClO氧化,反应的离子方程式为______________________。
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外还有_______________。
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:____________________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度/℃ | 40 | 50 | 60 | 70 |
S(MgSO4)/g | 30.9 | 33.4 | 35.6 | 36.9 |
S(CaSO4)/g | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4的混合溶液中的CaSO4除去,根据上表数据,可确定操作步骤为蒸发结晶、________________(填操作名称)。
(6)实验中提供的硼镁泥共10 g,得到MgSO4·7H2O共17.22 g,则MgSO4·7H2O的产率为________。
【题目】根据所给的实验装置,下列有关实验的相关叙述正确的是
选项 | 实验装置 | 相关叙述 |
A |
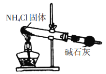
| 实验室可以用该装置和药品制取氨气 |
B |
| 反应过程中,温度降低,Ba(OH)2·8H2O与NH4Cl反应是吸热反应 |
C |
| ①中反应比②中快,说明温度升高可以加快反应速率 |
D |
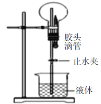
| 只有氨气等极易溶于水的气体才能利用该装置形成喷泉 |
A.AB.BC.CD.D