题目内容
【题目】有关元素X、Y、D、E的信息如下:
元素 | 有关信息 |
X | 地壳中含量最高的元素 |
Y | 第三周期中原子半径最小的元素 |
D | 最高价氧化物既能溶于强酸又能溶于强碱 |
E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
用化学用语回答下列问题:
(1)D在元素周期表中的位置为____。
(2)X、Y、D形成的简单离子的半径由大到小为_____。
(3)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为_________,D的单质溶于强碱的离子方程式为________。
(4)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)_____。
①保存EY2溶液时,需向溶液加入少量E单质
②EY2、EY3均能通过化合反应生成
③向煮沸的NaOH溶液中滴加几滴饱和EY3溶液,可以制得胶体
【答案】第三周期第ⅢA族 r(Cl-)>r(O2-)>r(Al3+) 2H2O2![]() 2H2O+O2↑ 2Al+2OH-+2H2O=2A1O2-+3H2↑ ①②
2H2O+O2↑ 2Al+2OH-+2H2O=2A1O2-+3H2↑ ①②
【解析】
X是地壳中含量最高的元素,则其为氧(O);Y为第三周期中原子半径最小的元素,则其为氯(Cl);D元素的最高价氧化物既能溶于强酸又能溶于强碱,则其为铝(Al);E的单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏,则其为铁(Fe)。
(1)铝的原子结构示意图为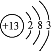 ,则其在元素周期表中的位置为第三周期第ⅢA族;
,则其在元素周期表中的位置为第三周期第ⅢA族;
(2)比较O2-、Al3+、Cl-的半径时,O2-、Al3+为两个电子层数,Cl-为三个电子层,则Cl-半径最大,O2-、Al3+的核电荷数,前者为8后者为13,所以离子半径前者大于后者,从而得出离子半径大小关系为r(Cl-)>r(O2-)>r(Al3+);
(3)X的一种氢化物可用于实验室制取X的单质,则其为H2O2,其反应的化学方程式为2H2O2![]() 2H2O+O2↑,Al的单质溶于强碱离子的离子方程式为2Al+2OH-+2H2O=2A1O2-+3H2↑;
2H2O+O2↑,Al的单质溶于强碱离子的离子方程式为2Al+2OH-+2H2O=2A1O2-+3H2↑;
(4)①保存FeCl2溶液时,需向溶液加入少量Fe单质,以防止Fe2+被空气中O2氧化,①正确;
②FeCl2可由Fe与FeCl3化合制得,FeCl3可由Fe与Cl2化合制得,②正确;
③向煮沸的NaOH溶液中滴加1~2mL饱和FeCl3溶液,并继续煮沸至液体呈红褐色,可以制得胶体,③错误;
故选①②。