题目内容
20.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.用下面的反应可制取K2FeO4:2Fe(OH)3+3Cl2+10KOH$\frac{\underline{\;0-20℃\;}}{\;}$2K2FeO4+6KCl+8H2O,对于该反应,下列说法正确的是( )| A. | Cl2作氧化剂,发生还原反应 | |
| B. | 钾元素化合价降低 | |
| C. | 该反应是置换反应 | |
| D. | 每生成2 mol K2FeO4,转移3 mol电子 |
分析 2Fe(OH)3+3Cl2+10KOH$\frac{\underline{\;0-20℃\;}}{\;}$2K2FeO4+6KCl+8H2O反应中,Cl元素的化合价从0价降低到-1价,Cl2得电子作氧化剂,Fe元素的化合价从+3价升高到+6价,Fe(OH)3失电子作还原剂,据此分析.
解答 解:A.反应中,Cl元素的化合价从0价降低到-1价,Cl2得电子作氧化剂,发生还原反应,故A正确;
B.反应中钾元素的化合价不变,故B错误;
C.一种单质与一种化合物反应生成另一种单质和另一种化合物的反应为置换反应,该反应不是置换反应,故C错误;
D.Fe元素的化合价从+3价升高到+6价,每生成1 mol K2FeO4,转移3 mol电子,故D错误.
故选A.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
10.某有机物A可用于合成药物达菲,其结构简式如图,下列关于A的说法不正确的是( )


| A. | 分子式为C7H6O5 | |
| B. | 和溴水既可以发生取代反应,又可以发生加成反应 | |
| C. | 1 mol该化合物最多可以与含4 mol NaOH的溶液反应 | |
| D. | 既可以和FeCl3溶液发生显色反应,又可以和NaHCO3溶液反应放出CO2气体 |
8.工业上,下列金属冶炼需要采用电解法的是( )
| A. | Ag | B. | Cu | C. | Fe | D. | Mg |
15.设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol 甲基(-CH3)中含有的电子总数为NA | |
| B. | 标准状况下,11.2 L乙醇所含碳原子数目为NA | |
| C. | 常温常压下,26 g 苯中所含的碳碳双键数为NA | |
| D. | 23g钠在足量氧气充分燃烧,转移电子数为NA |
12.已知鲨烯分子含有30个C原子及6个C=C且不含环状结构,则其分子式为( )
| A. | C30H50 | B. | C30H52 | C. | C30H56 | D. | C30H60 |
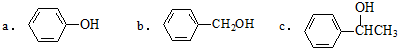
9.下列化合物在1H-NMR中出现三组特征峰的是( )
| A. | 2一甲基一2一丁烯 | B. | 3,3一二甲基一2一丁醇 | ||
| C. | 4一甲基苯酚 | D. | 2,3,4一三甲基戊烷 |
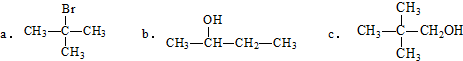
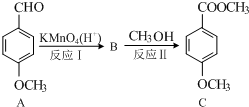
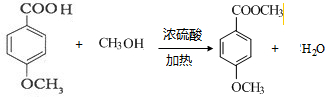 .
.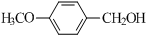 与O2反应制得,写出该反应的化学方程式
与O2反应制得,写出该反应的化学方程式 .
.