题目内容
【题目】常温下,二元弱酸 H2Y 溶液中滴加 NaOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如图所示,下列有关说法错 误的是( )
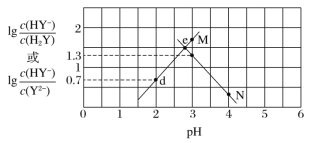
A.曲线 M 表示 pH 与 lgc(HY-)/c(H2Y)的变化关系
B.Ka2(H2Y)=10-4.3
C.d 点溶液中:c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(Na+)
D.交点 e 的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
【答案】D
【解析】
A. pH增大,表示溶液中碱性增强,溶液中H2Y减少,HY-增多,据此判断变化关系;
B. 曲线N表示lg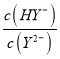 ,Ka2(H2Y)=
,Ka2(H2Y)=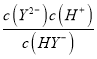 ,根据图像计算;
,根据图像计算;
C.根据电荷守恒分析;
D.交点e表示lg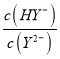 = lg
= lg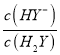 ,即c(Y2-)=c(H2Y),根据图像进行分析;
,即c(Y2-)=c(H2Y),根据图像进行分析;
A. pH增大,表示溶液中碱性增强,溶液中H2Y减少,HY-增多,因此lg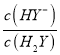 增大,则曲线M表示pH与lg
增大,则曲线M表示pH与lg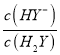 的变化关系,A项正确,不符合题意;
的变化关系,A项正确,不符合题意;
B. 曲线N表示lg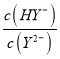 ,当pH=3时,lg
,当pH=3时,lg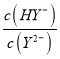 =1.3,则Ka2(H2Y)=
=1.3,则Ka2(H2Y)=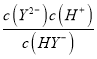 =10-3×10-1.3=10-4.3,B项正确,不符合题意;
=10-3×10-1.3=10-4.3,B项正确,不符合题意;
C. 溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HY-)+2c(Y2-),因此c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(Na+),C项正确,不符合题意;
D. 交点e表示lg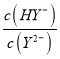 = lg
= lg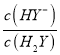 ,即c(Y2-)=c(H2Y),根据图像可知此时lg
,即c(Y2-)=c(H2Y),根据图像可知此时lg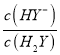 >1,所以c(HY-) >c(H2Y)=c(Y2-),D项错误,符合题意;
>1,所以c(HY-) >c(H2Y)=c(Y2-),D项错误,符合题意;
答案选D。

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案
相关题目