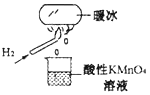
��Ŀ����
����Ŀ���ظ����[(NH4)2Cr2O7]���������Լ���������ýȾ���ȡ�ʵ���ҳ����ü�ȩ���ⶨ�ظ������Ʒ�е��������������䷴Ӧԭ��Ϊ2Ba2++Cr2O72+H2O = 2BaCrO4��+2H+��4NH4++6HCHO = 3H++6H2O+(CH2)6N4H+ [�ζ�ʱ��1 mol (CH2)6N4H+��1 mol H+�൱]��Ȼ����NaOH����Һ�ζ���Ӧ���ɵ��ᡣ
ʵ�鲽�裺��ȡ��Ʒ2.800 g�����250 mL��Һ����ȡ25.00 mL��Ʒ��Һ����ƿ�У��������ᱵ��ҺʹCr2O72��ȫ��������10 mL 20%�����Լ�ȩ��Һ��ҡ�ȣ�����5 min����1~2�η�̪��Һ����0.200 mol��L-1 NaOH����Һ�ζ����յ㣬�ظ���������3�Ρ��ζ�������±���ʾ��
�ζ����� | ������Һ�����/mL | ����Һ����� | |
�ζ�ǰ�̶�/mL | �ζ���̶�/mL | ||
1 | 25.00 | 1.05 | 21.06 |
2 | 25.00 | 1.98 | 21.97 |
3 | 25.00 | 0.20 | 21.98 |
����Ʒ�е�����������Ϊ_________(���������λС��)����д����Ҫ��������̡�
���𰸡�10.00% (NH4)2Cr2O7 ��2N �� 4 H+ ��4NaOH�õ�n(N) =![]() n(NaOH) =
n(NaOH) =![]() ��0.200mol��L-1��0.02L��10=0.02mol��������������
��0.200mol��L-1��0.02L��10=0.02mol��������������![]()
��������
�ȼ�������NaOH����Һ�������ƽ��ֵ���ٸ��ݹ�ϵʽ(NH4)2Cr2O7 ��2N �� 4 H+ ��4NaOH���м��㵪������������
�����������Ʊ���Һ������ֱ�Ϊ��20.01mL��19.99mL��21.78mL�����̫����ȥ��������ƽ������V(NaOH)=20.00mL�����ݹ�ϵʽ(NH4)2Cr2O7 ��2N �� 4 H+ ��4NaOH�õ�n(N) = ![]() n(NaOH)=
n(NaOH)=![]() ��0.200mol��L-1��0.02L��10=0.02mol��������������
��0.200mol��L-1��0.02L��10=0.02mol��������������![]() ��
��
�ʴ�Ϊ��10.00%��(NH4)2Cr2O7 ��2N �� 4 H+ ��4NaOH�õ�n(N) =![]() n(NaOH) =
n(NaOH) =![]() ��0.200 mol��L-1��0.02L ��10 = 0.02mol��������������
��0.200 mol��L-1��0.02L ��10 = 0.02mol��������������![]() ��
��