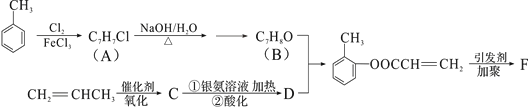
题目内容
【题目】(1)下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各问题。
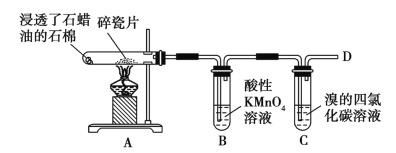
①B中溶液褪色,是因为乙烯被______________。
②C中发生反应的化学方程式为_________________________。
③在D处点燃时必须进行的操作是_____________。
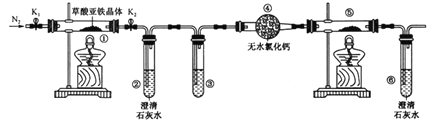
(2)实验室制取的乙烯中常混有少量的SO2,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
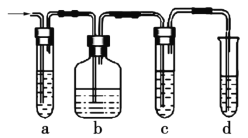
①图中a、b、c、d装置盛放的试剂依次是___(填序号)。
A.品红溶液
B.NaOH溶液
C.浓硫酸
D.酸性高锰酸钾溶液
②能说明SO2存在的实验现象是_____________。
③使用装置b的目的是_____________。
④使用装置c的目的是_____________。
⑤能证明混合气体中含有乙烯的现象是________________________________。
【答案】酸性KMnO4溶液氧化 CH2=CH2+Br2![]()
![]() 检验气体的纯度 A、B、A、D 装置a中品红溶液褪色 除去SO2气体,以免干扰乙烯的检验实验 检验SO2气体是否除尽 装置c中品红溶液不褪色,装置d中酸性高锰酸钾溶液褪色
检验气体的纯度 A、B、A、D 装置a中品红溶液褪色 除去SO2气体,以免干扰乙烯的检验实验 检验SO2气体是否除尽 装置c中品红溶液不褪色,装置d中酸性高锰酸钾溶液褪色
【解析】
石蜡分解生成的气体中含有乙烯,乙烯能使酸性高锰酸钾溶液褪色,乙烯和溴的四氯化碳溶液发生加成反应。乙烯和二氧化硫都可以使酸性高锰酸钾溶液褪色,但是二氧化硫能使品红褪色,且能和氢氧化钠反应,乙烯不能,所以可以先用品红检验二氧化硫的存在,然后用氢氧化钠吸收除去二氧化硫,再次用品红检验二氧化硫已经除净,最后用酸性高锰酸钾溶液检验乙烯。
(1) ①B中为酸性高锰酸钾溶液,乙烯能被酸性KMnO4溶液氧化而使高锰酸钾溶液褪色。 ②乙烯和溴发生加成反应,方程式为:CH2=CH2+Br2![]()
![]() 。③乙烯是可燃性气体,点燃前先检验气体的纯度。 (2) ①乙烯和二氧化硫的混合气体进行检验时,先用品红检验二氧化硫,然后用氢氧化钠溶液除去二氧化硫,再用品红检验二氧化硫已经除净,最后用酸性高锰酸钾溶液检验乙烯,所以试剂的盛放顺序为 A、B、A、D 。 ② 装置a中品红溶液褪色可以证明二氧化硫的存在。③氢氧化钠溶液的目的是除去SO2气体,以免干扰乙烯的检验实验。④再次通入品红是为了检验SO2气体是否除尽。⑤装置c中品红溶液不褪色,证明不含有二氧化硫,装置d中酸性高锰酸钾溶液褪色,说明气体为乙烯。
。③乙烯是可燃性气体,点燃前先检验气体的纯度。 (2) ①乙烯和二氧化硫的混合气体进行检验时,先用品红检验二氧化硫,然后用氢氧化钠溶液除去二氧化硫,再用品红检验二氧化硫已经除净,最后用酸性高锰酸钾溶液检验乙烯,所以试剂的盛放顺序为 A、B、A、D 。 ② 装置a中品红溶液褪色可以证明二氧化硫的存在。③氢氧化钠溶液的目的是除去SO2气体,以免干扰乙烯的检验实验。④再次通入品红是为了检验SO2气体是否除尽。⑤装置c中品红溶液不褪色,证明不含有二氧化硫,装置d中酸性高锰酸钾溶液褪色,说明气体为乙烯。