题目内容
【题目】如图是利用试纸、铅笔芯设计的微型实验.以铅笔芯为电极,分别接触表面皿上的试纸,接通电源,观察实验现象.下列说法错误的是( )
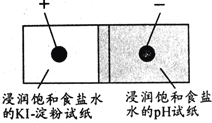
A.pH试纸变蓝
B.KI﹣淀粉试纸变蓝
C.通电时,电能转换为化学能
D.电子通过pH试纸到达KI﹣淀粉试纸
【答案】D
【解析】
A.连接负极的铅笔芯为阴极,阴极上氢离子放电生成氢气,同时电极附近生成氢氧根离子,溶液呈碱性,pH试纸遇碱变蓝色,故A正确;
B.连接正极的铅笔芯为阳极,阳极上氯离子放电生成氯气,氯气能氧化碘离子生成碘,碘与淀粉试液变蓝色,所以淀粉碘化钾试纸变蓝色,故B正确;
C.该装置是将电能转化为化学能装置,为电解池,故C正确;
D.电子不通过电解质溶液,电解质溶液中阴阳离子定向移动形成电流,故D错误;
故答案为D。

【题目】活性氧化锌是一种多功能性的新型无机材料.某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:
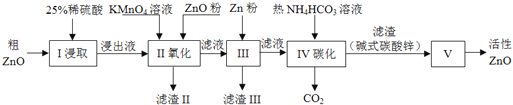
已知各相关氢氧化物沉淀pH范围如下表所示:
Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
完成下列填空
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯外,还需要_______(选填编号)
A.电子天平 B.量筒 C.容量瓶 D.胶头滴管
(2)步骤II中通过加入KMnO4氧化,并用ZnO调节pH,可以除去含铁杂质.检验沉淀是否完全的实验操作是_________.调节pH的适宜范围是_________.
(3)步骤III中加入Zn粉的作用是:①________;②进一步调节溶液pH.
(4)步骤IV中使用热NH4HCO3溶液能促进Zn2+转化为沉淀,但温度不宜过高,其原因可能是________.
(5)步骤V在_______(填仪器名称)中进行,已知碱式碳酸锌的化学式为Zn5(OH)6(CO3)2,请写出发生反应的化学方程式:________.判断已分解完全的操作是________.
(6)用如下方法测定所得活性氧化锌的纯度:
①取1.000g活性氧化锌,用15.00mL 1.000mol/L硫酸溶液完全溶解
②用浓度为0.500mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL.
假设杂质不参与反应,则所得活性氧化锌的纯度为_______.若在滴定时,实际操作中过量半滴(1mL溶液为25滴),则本次滴定的相对误差为_____.
【题目】如图,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行下列实验:

下列说法正确的是( )
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 乙针筒里的现象 |
A | H2S | CuSO4溶液 | 产生黑色沉淀 |
B | H2S | FeSO4溶液 | 产生黑色沉淀 |
C | SO2 | H2S | 出现淡黄色固体 |
D | SO2 | 紫色石蕊溶液 | 先变红后褪色 |
A.AB.BC.CD.D
【题目】室温时几种物质的溶解度见下表。室温下,向500g硝酸钾饱和溶液中投入2g食盐,下列推断正确的是( )
物质 | 溶解度( g/100g水) |
氯化钠 | 36 |
硝酸钾 | 32 |
硝酸钠 | 87 |
氯化钾 | 37 |
A.食盐不溶解
B.食盐溶解,无晶体析出
C.食盐溶解,析出2 g硝酸钾晶体
D.食盐溶解,析出2 g氯化钾晶体