题目内容
【题目】向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如下图所示。
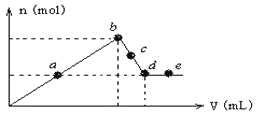
则下列说法正确的是( )
A.a、c两点沉淀物成份相同,d、e两点沉淀物成份相同
B.b—c段与c—d段溶液中阴离子的物质的量相等
C.在d点,向溶液中加入盐酸,沉淀量将减少
D.在反应过程中,各状态点溶液的pH大小顺序是:e > d > c > a > b
【答案】A
【解析】
A.a、c两点沉淀物成份相同,均是Mg(OH)2和Al(OH)3的混合物,d、e两点沉淀物成份相同,均为Mg(OH)2,正确;
B.b—c段与c—d段溶液中阴离子的物质的量不相等,Cl―不变,AlO2―从b→d增加,不正确;
C.在d点,向溶液中加入盐酸,沉淀量将增加,AlO2―+H++H2O="Al" (OH)3↓,不正确;
D.从溶液中的物质可以分析出a MgCl2和AlCl3酸性;b、NaCl 中性;c.NaAlO2呈碱性,但浓度小;d.NaAlO2浓度大碱性增强;e、NaAlO2、NaOH 碱性最强。所以在反应过程中,各状态点溶液的pH大小顺序是:e > d > c > b > a,不正确;
选A。

练习册系列答案
相关题目