题目内容
1L稀硝酸和稀硫酸的混合溶液,其溶质的物质的量浓度分别为0.1mol/L 和0.2mol/L。若向该混合溶液中加入足量的铜粉。则最多能溶解铜粉的质量为
| A.2.4 g | B.3.2 g | C.6.4 g | D.9.6 g |
D
解析试题分析:发生3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,n(H+)=0.5mol,n(NO3-)=0.1mol,氢离子过量,故能溶解0.15mol铜,质量为9.6g。
考点:化学计算,元素及化合物知识。

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.在密闭容器中加入1.5molH2和0.5molN2,充分反应后可得NH3分子数目为NA |
| B.1.0L 0.1mol?L—1Na2CO3溶液中含有的CO32—离子数目为0.1NA |
| C.一定条件下,2.3gNa完全与O2反应生成3.6g产物时失去电子数目为0.1NA |
| D.在标准状况下,2.24L的CH3CH2OH含有NA个分子 |
下列说法正确的是
| A.7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.2×6.02×1023 |
| B.标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.0×6.02×1023 |
| C.2.24LSO2与O2混合气体中所含氧原子数为0.2×6.02×1023 |
| D.Vlamol·L-1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023 |
在100 mL某浓度的NaOH溶液中通入一定量的CO2气体,得到溶液X,再向溶液X中逐滴加入0.1mol/L的盐酸,产生的气体体积与加入盐酸的体积关系如下图所示,有关说法错误的是( )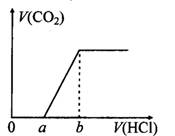
| A.若a:b<1:2,则0~a段发生的离子反应为:CO32-+H+= HCO3- |
| B.若a:b>l:2,且b="20" mL,则原NaOH溶液的浓度为0.02 mol/L |
| C.若a:b=1:2,则溶液X中离子浓度满足:c(H+)+c(HCO3-)=c(OH-)-c(H2CO3) |
| D.a:b为任意值时,溶液X中离子浓度均满足:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解(产生气体全部逸出),冷却后将溶液稀释至1000ml,测得c(H+)=0.84mol/L;若要使稀释后溶液中的Cu2+沉淀完全,应加入6.0mol/L的NaOH溶液的体积为
| A.100mL | B.160mL | C.240mL | D.307mL |
FeS2在空气中充分燃烧的化学方程式为4FeS2 + 11O2 2Fe2O3 + 8SO2,若agFeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
2Fe2O3 + 8SO2,若agFeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
| A.120N/a | B.120a/11N | C.11a/120N | D.120N/11a |
有关碳元素及其化合物的化学用语正确的是
A.CO2的电子式: |
B.C原子最外层电子的轨道表示式: |
| C.醋酸钠的分子式:C2H3O2Na |
D.乙烯的比例模型: |
下列化学用语正确的是
A.乙烯的比例模型: |
| B.HClO的结构式为:H—Cl—O |
C.H2O2的电子式: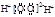 |
| D.乙醇的分子式:CH3CH2OH |