题目内容
15.化学键的键能是原子间形成1mol化学键(或其逆过程)时释放(或吸收)的能量.以下是部分共价键键能的数据:H-S:364kJ•mol-1,S-S:266kJ•mol-1,S═O:522kJ•mol-1,H-O:464kJ•mol-1.
(1)试根据这些数据计算下面这个反应的反应热:
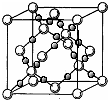
2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-Q kJ•mol-1,反应产物中的S实为S8,实际分子是一个8元环状分子(即
 ),则Q=154.
),则Q=154.(2)标准状况下,将a L H2S与b L SO2混合进行上述反应,当a>2b时,反应放热$\frac{154b}{22.4}$kJ•mol-1.
(3)又已知H2O(l)=H2O(g)△H=+44kJ•mol-1请写出(1)中反应若生成气态水时的热化学方程式2H2S(g)+SO2(g)=3S(s)+2H2O(g)△H=-66 kJ•mol-1.
分析 (1)根据2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-Q kJ•mol-1,反应产物中的S实为S8,将方程变形为:2H2S(g)+SO2(g)=$\frac{3}{8}$S8(s)+2H2O(l)△H=-Q kJ•mol-1,根据△H=反应物的总键能-生成物的总键能计算;
(2)根据2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-Q kJ•mol-1,当a>2b时,硫化氢过量,依据二氧化硫计算;
(3)1mol液态水变成气态水需吸热44KJ,若2mol液态水变成水蒸气时则吸热88KJ,结合2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-Q kJ•mol-1求解.
解答 解:(1)2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-Q kJ•mol-1,反应产物中的S实为S8,将方程变形为:2H2S(g)+SO2(g)=$\frac{3}{8}$S8(s)+2H2O(l)△H=-Q kJ•mol-1,2 mol H2S中有4 mol H-S键,1 mol SO2中有2 mol S=O键,3 mol S中有$\frac{3}{8}$mol S8,即3mol S-S键,2 mol H2O中有4 mol H-O键,根据△H=反应物的总键能-生成物的总键能=(4×364+2×522-3×266-4×464 )kJ/mol=-154 kJ/mol,
故答案为:154;
(2)根据2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-Q kJ•mol-1,当a>2b时,硫化氢过量,SO2不足,以SO2的量计算,SO2有 $\frac{b}{22.4}$mol,放热$\frac{b}{22.4}$×154KJ=$\frac{154b}{22.4}$kJ,故答案为:$\frac{154b}{22.4}$;
(3)1mol液态水变成气态水需吸热44KJ,若2mol液态水变成水蒸气时则吸热88KJ,根据2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-154 kJ•mol-1,生成气态水时共放热(154-88)KJ=66KJ,则热化学方程式为:2H2S(g)+SO2(g)=3S(s)+2H2O(g)△H=-66 kJ•mol-1,
故答案为:2H2S(g)+SO2(g)=3S(s)+2H2O(g)△H=-66 kJ•mol-1.
点评 本题考查反应热的有关计算、键能与反应热的关系等,为高频考点,侧重于学生的分析能力和计算能力的考查,明确反应热和键能的关系△H=反应物的总键能-生成物的总键能是解题关键,题目难度中等.

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案| A. | 与HCl加成生成CH3COCl | B. | 与H2O加成生成CH3COOH | ||
| C. | 与CH3COOH加成生成CH3COOCOCH3 | D. | 与CH3OH加成生成CH3COCH2OH |
| A. | Mg | B. | Al | C. | Si | D. | Cl2 |
| A. | 受热时Na2CO3比NaHCO3稳定 | |
| B. | 同温同压下,在水中Na2CO3比NaHCO3溶解性小 | |
| C. | 物质的量相等的Na2CO3和NaHCO3分别溶于等体积的水后,Na2CO3水溶液的碱性较弱 | |
| D. | 质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,Na2CO3放出的CO2少 |
| A. | 非金属性:P<S<O<F | B. | 原子半径大小:Na>S>O | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 还原性强弱:F->Cl->I- |
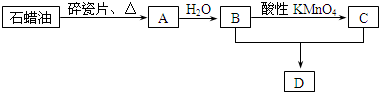
 CH3CH2OH反应类型是加成反应;B+C→D的化学方程式为:CH3COOH+C2H5OH
CH3CH2OH反应类型是加成反应;B+C→D的化学方程式为:CH3COOH+C2H5OH  CH3COOC2H5+H2O.反应类型是酯化反应或取代反应;
CH3COOC2H5+H2O.反应类型是酯化反应或取代反应;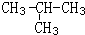 .
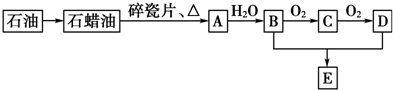
.
 ,它的一氯取代产物有2种.
,它的一氯取代产物有2种.
 已知A、B、C、D、E五种元素的原子序数依次增大,其中A、E原子的最外层电子数均等于其周期序数,E原子的电子层数是A的3倍;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子.请回答下列问题:
已知A、B、C、D、E五种元素的原子序数依次增大,其中A、E原子的最外层电子数均等于其周期序数,E原子的电子层数是A的3倍;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子.请回答下列问题: