题目内容
7.在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体[(NH4)2SO4•FeSO4•6H2O](式量为392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.(1)为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D.
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
(2)为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
分析 (1)依据该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇分析,洗涤不能溶解产品,不能引入新的杂质;
(2)称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定,发生的反应为高锰酸钾溶液氧化亚铁离子为铁离子;
反应终点的判断可以利用高锰酸钾溶液的紫红色判断,滴入最后一滴溶液变化为紫红色,半分钟内不变,证明反应达到终点;
依据反应的定量关系计算亚铁离子物质的量,得到(NH4)2SO4•FeSO4•6H2O的质量,计算纯度,高锰酸钾溶液的体积第一次误差较大,应舍去;
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积,液面被提高,读取体积减小;
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡测定溶液体积增大;
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,待装液润洗会增多消耗高锰酸钾溶液的体积,测定结果增大;
D.三次使用的高锰酸钾都是一样的,消耗的高锰酸钾体积应是相同的.
解答 解:(1)因为硫酸亚铁铵易溶于水,不溶于乙醇,应该用乙醇洗涤,减少硫酸亚铁铵的溶解,同时利用乙醇和水互溶,从而达到洗涤的要求,故选D,
故答案为:D;
②利用高锰酸钾的强氧化性,Fe2+的强还原性,两者发生氧化还原反应,Fe2+被氧化成Fe3+↑1,Mn由+7价→+2↓5,最小公倍数5,根据原子个数、电荷守恒,即MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,向溶液中滴加中高锰酸钾,高锰酸钾显紫红色,因此滴定到终点:最后一滴滴入,溶液由无色变为浅紫色,且30s不变色,因为第一次与第二次、第三次相差较大,忽略不计,消耗高锰酸钾溶液的体积为$\frac{25.02+24.98}{2}$ml=25mL,根据离子反应方程式,得出:n[(NH4)2SO4•FeSO4•6H2O]=5n(KMnO4)=25×10-3×c×5mol,则500mL溶液中含有n[(NH4)2SO4•FeSO4•6H2O]=25×10-3×c×5×500/25mol=2.5cmol,
所以质量分数=2.5c×$\frac{392}{a}$×100%=$\frac{980c}{a}$×100%,
A、俯视读数,造成所读的数偏小,故A错误;
B、滴定管尖嘴有气泡,滴定结束无气泡,所消耗的液体体积增加,故B正确;
C、锥形瓶用待测液润洗,待测液的物质的量增加,则消耗高锰酸钾的体积增加,故C正确;
D、三次使用的高锰酸钾都是一样的,消耗的高锰酸钾体积应是相同的,故D错误.
故选BC,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;滴入最后一滴高锰酸钾溶液,锥形瓶内溶液由浅绿色变为浅紫色,且30s不变色;$\frac{980c}{a}$×100%;BC.
点评 本题考查了氢氧化亚铁制备的非常规制备方法和实验过程分析判断,滴定实验的注意问题和计算应用,注意掌握物质性质,实验过程的理解应用,掌握基础是解题关键,题目难度中等.

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案| A. | 500 mL 1 mol/L的HNO3溶液 | B. | 1 L 0.5 mol/L的Fe(NO3)3溶液 | ||
| C. | 100 mL 0.5 mol/L的Mg(NO3)2溶液 | D. | 300 mL 1 mol/L的Mg(NO3)2溶液 |
| A. | Na2CO3→NaHCO3 | B. | Fe→FeCl2 | C. | NaCl→Na | D. | Al2O3→Al(OH)3 |
| A. | 1mol Na2O2中所含的离子数目为3NA | |
| B. | 标况下,22.4L氯气参与的反应中,转移的电子数一定为2NA | |
| C. | 0.1mol/L Al2(SO4)3溶液中,Al3+的数目为0.2NA | |
| D. | 1molSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |
| A. | K+、MnO4-、S2-、SO42- | B. | K+、OH-、Cl-、CO32- | ||
| C. | Ca2+、CH3COO-、Al3+、SO42- | D. | Na+、Ba2+、Cl-、NO3- |
| A. | CO2的分子模型示意图: | |
| B. | 氯化铵的电子式: | |
| C. | 硫离子的核外电子排布式 1s22s22p63s23p4 | |
| D. | NH3、H2O、CO2、HCl四分子中孤电子对最多的是CO2 |
| A. | 用手接触药品 | B. | 用嘴吹熄酒精灯火焰 | ||
| C. | 点燃氢气前一定要检验氢气的纯度 | D. | 将带有溶液的滴管平放在实验台上 |
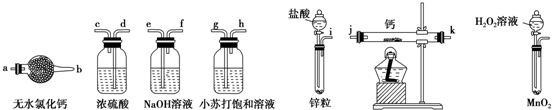
 .
.