题目内容
【题目】下列关于反应与能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) ΔH=-216kJ·mol-1,E反应物<E生成物
B.CaCO3(s)=CaO(s)+CO2(g) ΔH=+178.2kJ·mol-1,E反应物<E生成物
C.2HCl(g)=H2(g)+Cl2(s) ΔH=+92.3kJmol-1,1molHCl在密闭容器中分解后放出92.3kJ的能量
D.将0.5molN2和1.5molH2置于密闭的容器中充分反应后生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ·mol-1
2NH3(g) ΔH=-38.6kJ·mol-1
【答案】B
【解析】
A. 反应物的总能量大于生成物的总能量为放热反应;
B. 反应物的总能量小于生成物的总能量为吸热反应;
C. 该反应为吸热反应;
D. 该反应为可逆反应。
A.当反应物总能量<生成物总能量,则反应是吸热反应,但该反应ΔH<0,A项错误;
B.当反应物总能量<生成物总能量,则反应是吸热反应,该反应ΔH>0,B项正确;
C.根据热化学方程式2HCl(g)=H2(g)+Cl2(s) ΔH=+92.3kJ·mol-1可知HCl分解是吸热反应,C项错误;
D.反应N2(g)+3H2(g)![]() 2NH3(g)是可逆反应,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g)小于1.0mol,放热19.3kJ,则热化学方程式应为N2(g)+3H2(g)
2NH3(g)是可逆反应,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g)小于1.0mol,放热19.3kJ,则热化学方程式应为N2(g)+3H2(g)![]() 2NH3(g) ΔH<-38.6kJ·mol-1,D项错误;
2NH3(g) ΔH<-38.6kJ·mol-1,D项错误;
答案选B。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】某实验探究小组研究320K时![]() 的分解反应:
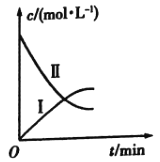
的分解反应:![]() 。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
t/min | 0 | 1 | 2 | 3 | 4 |
| 0.160 | 0.114 | 0.080 | 0.056 | 0.040 |
| 0 | 0.023 | 0.040 | 0.052 | 0.060 |
A.曲线Ⅰ是![]() 的浓度变化曲线
的浓度变化曲线
B.曲线Ⅱ是![]() 的浓度变化曲线
的浓度变化曲线
C.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快
D.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快