题目内容
4.关于配制一定物质的量浓度溶液的说法,正确的组合是( )①托盘天平可读取到小数点后一位(以克为单位)
②托盘天平只能粗略地称量物质的质量,量筒只能粗略地量取液体的体积,严格地说,它们都不能与容量瓶--精确仪器配套使用
③量筒内的残液必须冲洗下来,倒入容量瓶中
④称量的固体(或量取的液体)可直接放入容量瓶中溶解(或稀释)
⑤引流时,玻璃棒不能靠在瓶口上
⑥定容摇匀后,若液面低于刻度线,可再次加水补充.
| A. | ①②⑤ | B. | ①③④ | C. | ②④⑥ | D. | ④⑤⑥ |
分析 ①托盘天平精确到0.1g;
②容量瓶是很精密的仪器;
③量筒内的残液要倒入废液缸;
④容量瓶不能受热;
⑤引流时,玻璃棒靠在瓶口上溶液导致溶液的溅出;
⑥定容摇匀后,若液面低于刻度线是正常的.
解答 解:①托盘天平精确到0.1g,即可读取到小数点后一位(以克为单位),故①正确;
②容量瓶是很精密的仪器,而托盘天平和量筒相对较粗略,故②正确;
③量筒内的残液要倒入废液缸,如果要注入容量瓶中,会导致溶质质量偏多,则所配溶液浓度偏高,故③错误;
④容量瓶不能受热,故不能用于溶解固体或稀释溶液,故④错误;
⑤引流时,玻璃棒靠在瓶口上溶液导致溶液的溅出,故玻璃棒不能靠在瓶口上,故⑤正确;
⑥定容摇匀后,若液面低于刻度线是正常的,若再加水,则溶液的浓度将偏低,故⑥错误.
故选A.
点评 本题考查了一定物质的量浓度溶液的配制,注意从c=$\frac{n}{V}$理解配制原理,注意量筒的精确度为0.1,题目难度不大.

练习册系列答案
相关题目
14.下列离子方程式书写正确的是( )
| A. | 硝酸银溶液中加入铜粉:Ag++Cu═Cu2++Ag | |
| B. | Ba(OH)2与稀H2SO4反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 向澄清石灰水中通入足量二氧化碳:OH-+CO2═HCO3- | |
| D. | 碳酸钙溶于醋酸中:CaCO3+2H+═Ca2++2H2O+CO2↑ |
15.反应4NH3+5O2?4NO+6H2O在一定体积的密闭容器中进行,30s后NO的物质的量浓度增加了3mol/L,则下列反应速率正确的是( )
| A. | v(NO)=0.01mol•(L•s)-1 | B. | v(NO)=0.02mol•(L•s)-1 | ||
| C. | v(NH3)=0.1mol•(L•s)-1 | D. | v(NH3)=0.2mol•(L•s)-1 |
12.下列说法中,正确的是( )
| A. | 具有较高能量的分子是活化分子 | |
| B. | 活化分子间的碰撞一定是有效碰撞 | |
| C. | 不同化学反应需要的活化能有可能差别很大 | |
| D. | 反应的活化能大小不会影响化学反应速率 |
9.常温下下列各组离子在给定条件下能大量共存的是( )
| A. | 在pH=1的溶液中:NH4+、K+、ClO-、Cl- | |
| B. | pH<7的溶液中:SO42-、CO32-、Na+、K+ | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在c(H+)=1.0×10-13 mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- |
7.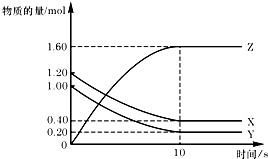 T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 平衡时X、Y的转化率相同 | |
| B. | 达到平衡后,将容器体积压缩为1L,平衡向正反应方向移动 | |
| C. | T℃时,该反应的化学方程式为:X(g)+Y(g)?2Z(g),平衡常数K=40 | |
| D. | T℃时,若起始时X为0.71mol,Y为1.00mol,则平衡时Y的转化率为60% |
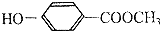 的同分异构体:
的同分异构体: