题目内容
14.如图所示,下列说法正确的是( )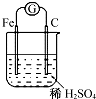
| A. | 铁电极的电极反应式为Fe-3e-═Fe3+ | |
| B. | 溶液中的H+移向Fe电极 | |
| C. | 该装置中能量转化方式为电能转化为化学能 | |
| D. | 电子从铁棒经导线流入石墨棒 |
分析 A、金属铁失电子生成亚铁离子;
B、原电池中,阳离子移向正极;
C、原电池是将化学能转化为电能的装置;
D、原电池中,电子从负极流向正极.
解答 解:A、金属铁是负极,铁电极的电极反应式为Fe-2e-═Fe2+,故A错误;
B、原电池中,电解质里的阳离子氢离子移向正极,即移向石墨电极,故B错误;
C、原电池是将化学能转化为电能的装置,故C错误;
D、原电池中,电子从负极流向正极,即从铁电极流向碳电极,故D正确.
故选D.
点评 本题考查学生原电池的工作原理以及电子移动方向等知识,注意基本知识的归纳和梳理是关键,难度中等.

练习册系列答案
相关题目
4.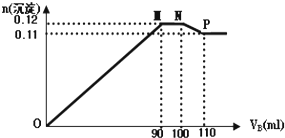 向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.
向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.
(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)BaSO4、Fe(OH)3
(2)从90mL至100 mL之间加入10mL B溶液时发生的离子反应方程式Al(OH)3+OH-=AlO2-+2H2O,Ba2++SO42-=BaSO4↓
(3)将A、B溶液中各溶质的物质的量浓度填入下表
 向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.
向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图.(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)BaSO4、Fe(OH)3
(2)从90mL至100 mL之间加入10mL B溶液时发生的离子反应方程式Al(OH)3+OH-=AlO2-+2H2O,Ba2++SO42-=BaSO4↓
(3)将A、B溶液中各溶质的物质的量浓度填入下表
| 溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
| C(mol/L) |
5.下列关于元素周期表的说法正确的是( )
| A. | 第2周期与第3周期元素从左到右,最高正化合价均从+1逐渐增大至+7,0族元素一般是0价 | |
| B. | 3个长周期所含元素种数相同 | |
| C. | 不同主族的3、4周期元素原子序数的差可能不同 | |
| D. | 同周期从左到右,非金属元素含氧酸的酸性逐渐增强 |
2.下列有关浓硝酸、稀硝酸反应的叙述不正确的是( )
| A. | 氧化性:浓硝酸大于稀硝酸 | |
| B. | 与相同质量的铜(反应完全)反应中转移的电子总数相同 | |
| C. | 与锌反应:前者生成NO2,后者生成H2 | |
| D. | 与铜反应:前者生成气体颜色深,后者生成气体颜色浅 |
19.下列关于有机物的叙述正确的是( )
| A. | 乙醇不能发生取代反应 | |
| B. | C4H10有三种同分异构体 | |
| C. | 乙二醇和丙三醇为同系物 | |
| D. | 乙烯和甲烷可用溴的四氯化碳溶液鉴别 |
6.设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下,32gO2含有2nA个氧原子 | |
| B. | 1mol Na2O2与足量水反应,转移2nA个电子 | |
| C. | 1L0.1mol•L-1Na2CO3溶液中含有0.1nA个CO${\;}_{3}^{2-}$ | |
| D. | 常温常压下,22.4LCH4中含有nA个CH4分子 |
3.下列物质中,不属于电解质的是( )
| A. | NaOH | B. | NaCl | C. | H2SO4 | D. | 盐酸 |
4.下列有关化学用语使用正确的是( )
| A. | CO2的电子式: | B. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | ||
| C. | 钾离子结构示意图: | D. | N原子的电子排布式:1s22s22p3 |