题目内容
4.下列有关化学用语使用正确的是( )| A. | CO2的电子式: | B. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | ||
| C. | 钾离子结构示意图: | D. | N原子的电子排布式:1s22s22p3 |
分析 A.二氧化碳分子中含有两个碳氧双键,不是碳氧单键;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
C.钾离子的核电荷数为19,不是18;
D.氮原子的核电荷数为7,核外电子总数为7,含有2个电子层,据此写出其电子排布式.
解答 解:A.二氧化碳为共价化合物,分子中存在碳氧双键,二氧化碳正确的电子式为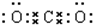 ,故A错误;
,故A错误;
B.核内有8个中子的碳原子的质量数为14,该核素的正确表示方法为:614C,故B错误;
C.钾离子的核电荷数为19,核外电子总数为18,其正确的离子结构示意图为: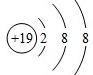 ,故C错误;
,故C错误;
D.N原子的核外电子总数为7,期电子排布式为:1s22s22p3,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子排布式、离子结构示意图、电子式、元素符号等知识,明确常见化学用语的书写原则为解答关键.

练习册系列答案
相关题目
14.如图所示,下列说法正确的是( )
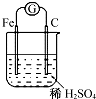

| A. | 铁电极的电极反应式为Fe-3e-═Fe3+ | |
| B. | 溶液中的H+移向Fe电极 | |
| C. | 该装置中能量转化方式为电能转化为化学能 | |
| D. | 电子从铁棒经导线流入石墨棒 |
15.滴定实验是化学学科中最重要的定量实验之一.常见的滴定实验有酸碱中和滴定、氧化还原反应滴定、沉淀滴定等等.
(1)酸碱中和滴定--用标准盐酸滴定未知浓度的NaOH溶液.某学生的实验操作如下:
A.用碱式滴定管取稀NaOH 25.00mL,注入锥形瓶中,加入甲基橙做指示剂.
B.用待测定的溶液润洗碱式滴定管.
C.用蒸馏水洗净滴定管.
D.将酸式滴定管用标准的HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3cm处,赶气泡、调液面,再把滴定管固定好.
E.检查滴定管是否漏水.
F.另取锥形瓶,再重复操作一次.
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直,眼睛注视滴定管中液面的变化,并于终点时记下滴定管液面所在刻度.
上述操作步骤中有错误的是G(填写“序号”),若将错误更正,则整个滴定实验操作的正确顺序是ECBADGF或ECDBAGF(填写“序号”).
(2)氧化还原滴定--葡萄酒中抗氧化剂残留量的测定
葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
葡萄酒样品100.00mL$→_{蒸馏}^{盐酸}$馏分$→_{用0.01000mol/L标准I_{2}溶液滴}^{一定条件下,加入几点淀粉溶液}$…
注:实验中加入盐酸的目的:将Na2S2O5全部转化成SO2.
①滴定时,I2溶液应装在酸(“酸”或“碱”)式滴定管中,滴定终点时滴定现象是当滴入最后一滴碘溶液时,溶液由无色变为蓝色,且保持30s不变.
②实验消耗标准I2溶液25.00mL,所测样品中抗氧化剂的残留量(以游离SO2计算)为0.16g•L-1.
③上述滴定过程中的原理为SO2+I2+2H2O═SO42-+4H++2I-(用离子方程式表示),下列情形会造成测定结果偏高的是CD.
A.滴定持续时间稍长,溶液中部分HI被空气氧化
B.滴定前平视,滴定后俯视
C.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
(3)沉淀滴定--滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶.
参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是D(填选项字母).
A.NaCl B.NaBr C.NaCN D.Na2CrO4.
(1)酸碱中和滴定--用标准盐酸滴定未知浓度的NaOH溶液.某学生的实验操作如下:
A.用碱式滴定管取稀NaOH 25.00mL,注入锥形瓶中,加入甲基橙做指示剂.
B.用待测定的溶液润洗碱式滴定管.
C.用蒸馏水洗净滴定管.
D.将酸式滴定管用标准的HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3cm处,赶气泡、调液面,再把滴定管固定好.
E.检查滴定管是否漏水.
F.另取锥形瓶,再重复操作一次.
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直,眼睛注视滴定管中液面的变化,并于终点时记下滴定管液面所在刻度.
上述操作步骤中有错误的是G(填写“序号”),若将错误更正,则整个滴定实验操作的正确顺序是ECBADGF或ECDBAGF(填写“序号”).
(2)氧化还原滴定--葡萄酒中抗氧化剂残留量的测定
葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
葡萄酒样品100.00mL$→_{蒸馏}^{盐酸}$馏分$→_{用0.01000mol/L标准I_{2}溶液滴}^{一定条件下,加入几点淀粉溶液}$…
注:实验中加入盐酸的目的:将Na2S2O5全部转化成SO2.
①滴定时,I2溶液应装在酸(“酸”或“碱”)式滴定管中,滴定终点时滴定现象是当滴入最后一滴碘溶液时,溶液由无色变为蓝色,且保持30s不变.
②实验消耗标准I2溶液25.00mL,所测样品中抗氧化剂的残留量(以游离SO2计算)为0.16g•L-1.
③上述滴定过程中的原理为SO2+I2+2H2O═SO42-+4H++2I-(用离子方程式表示),下列情形会造成测定结果偏高的是CD.
A.滴定持续时间稍长,溶液中部分HI被空气氧化
B.滴定前平视,滴定后俯视
C.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
(3)沉淀滴定--滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶.
参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是D(填选项字母).
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
12.下列说法错误的是( )
| A. | 用稀硫酸可除去钢铁表面的铁锈 | |
| B. | 使用焰色反应可检验氯化钠中的钠离子 | |
| C. | 通过丁达尔效应可区分NaCl溶液和Al(OH)3胶体 | |
| D. | 向溶液中滴入硝酸银溶液产生白色沉淀,可证明含有Cl- |
19.分类是生活、学习和科学研究中常用的一种方法.下列物质的分类正确的是( )
| A. | 碳酸钠、碳酸钾、碳酸钙都属于可溶性的碳酸盐 | |
| B. | 盐酸、硫酸、硝酸都属于含氧酸 | |
| C. | 氢氧化钠、氢氧化钡、氢氧化钾都属于一元碱 | |
| D. | 生石灰、水、五氧化二磷都属于氧化物 |
13.有Fe、CuO和Fe2O3组成的混合物共mg,放人500mL1mol•L-1 HNO3溶液中,混合物完全溶解,生成2.24L(标准状况下)NO,再向反应后的溶液中加入200mL NaOH溶液,要使铁和铜元素完全沉淀下来,所加入的NaOH溶液的浓度最小是( )
| A. | 1mol•L-1 | B. | 1.5mol•L-1 | C. | 2mol•L-1 | D. | 2.5mol•L-1 |
