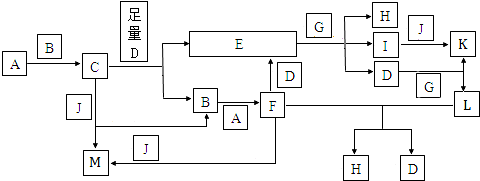
题目内容
9.两种化合物A和B,它们的分子中C、H、O原子个数的最简单整数比相同,但B的相对分子质量比A大.将264gA或B完全燃烧,都得到216gH2O和528gCO2.将等物质的量的A、B混合物0.33g完全气化测得气体体积折合为标准状况为112mL.求(1)化合物A和B的最简式C2H4O;
(2)A的分子式C2H4O;
(3)写出B的可能的二种结构简式CH3CH2CH2COOH,CH3CH2COOCH3.(要求不同类别的有机物)
分析 (1)根据n=$\frac{m}{M}$计算水、二氧化碳的物质的量,根据质量守恒计算氧元素质量,再计算氧原子物质的量,计算C、H、O原子数目之比,进而确定有机物最简式;
(2)计算平均摩尔质量,A的平均摩尔质量小于平均值,确定A的相对分子质量,进而确定A的分子式;
(3)结合平均相对分子质量计算B的相对分子质量,结合最简式确定分子式,书写可能的结构简式.
解答 解:(1)根据原子守恒n(H)=2n(H2O)=2×$\frac{216}{18g/mol}$=24mol,n(C)=n(CO2)=$\frac{528g}{44g/mol}$12mol,则氧元素质量=264g-24mol×1g/mol-12mol×12g/mol=96g,故n(O)=$\frac{96g}{16g/mol}$=6mol,则:n(C):n(H):n(O)=12mol:24mol:6mol=2:4:1,故A、B的最简式为C2H4O,故答案为:C2H4O;
(2)0.33g混合物的物质的量:$\frac{0.112L}{22.4L/mol}$=0.005mol,混合物的平均摩尔质量为:$\frac{0.33g}{0.005mol}$=66g/mol,相对分子质量较小的A只能是C2H4O,
故答案为:C2H4O;
(3)设B的相对分子质量为x,则$\frac{44+x}{2}$=66,解得x=88,所以B为C4H8O2,符合C4H8O2通式且是不同类别的可能的两种结构简式为:CH3CH2CH2COOH、CH3CH2COOCH3等,
故答案为:CH3CH2CH2COOH、CH3CH2COOCH3等.
点评 本题考查有机物分子式与结构式的确定,注意掌握分子式确定的方法,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下VL的x、y、z的混合气体可与V L的H2发生加成反应,则混合气体中x、y、z的体积比可能是( )
| A. | 1:1:1 | B. | 1:2:3 | C. | 1:4:2 | D. | 3:2:1 |
20.下列物质属于离子化合物的是( )
| A. | SiO2 | B. | CCl4 | C. | NaCl | D. | H2O |
4.下列反应中,硝酸只体现氧化性的是( )
| A. | CuO+HNO3 | B. | Cu+HNO3 | C. | FeO+HNO3 | D. | C+HNO3(浓) |
14.如图所示,下列说法正确的是( )
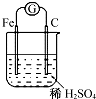

| A. | 铁电极的电极反应式为Fe-3e-═Fe3+ | |
| B. | 溶液中的H+移向Fe电极 | |
| C. | 该装置中能量转化方式为电能转化为化学能 | |
| D. | 电子从铁棒经导线流入石墨棒 |
1.下列事实不能用有机物分子内基团间的相互影响解释的是( )
| A. | 甲苯能使KMnO4酸性溶液褪色而苯和甲烷不能 | |
| B. | 苯酚能跟NaOH溶液反应而乙醇不能 | |
| C. | 乙烯能发生加成反应而乙烷不能 | |
| D. | 苯在50:60℃时发生硝化反应而甲苯在30℃时即可发生硝化反应 |
19.分类是生活、学习和科学研究中常用的一种方法.下列物质的分类正确的是( )
| A. | 碳酸钠、碳酸钾、碳酸钙都属于可溶性的碳酸盐 | |
| B. | 盐酸、硫酸、硝酸都属于含氧酸 | |
| C. | 氢氧化钠、氢氧化钡、氢氧化钾都属于一元碱 | |
| D. | 生石灰、水、五氧化二磷都属于氧化物 |