题目内容
2.氯化砜为无色或浅黄色发烟液体.易挥发,遇水分解,其制取过程的相关反应如下:S(s)+Cl2(g)$\frac{\underline{\;\;△\;\;}}{\;}$SCl2 (1)( I )
SCl2(1)+SO3(1)=S0Cl2(1)+SO2(g) ( II )
已知二氯化硫(SC12)熔点-78℃,沸点59℃,下图是实验室由氯气与硫合成二氯化硫的装罝.
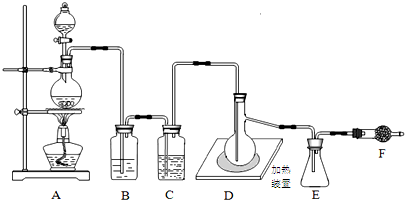
(1)仪器组装完成后,首先进行的一步操作是检查装置气密性;防止加热硫粉时;反应前要先排尽系统中空气,此做法目的是防止空气中的氧气与硫粉反应.
(2)装罝B盛放的药品是饱和氯化钠溶液,装罝D中玻璃仪器的名称是蒸馏烧瓶.
(3)实猃时,为防止E中液体挥发,可采取的措施是将锥形瓶放入冰水中冷却.装罝F(盛放碱石灰)有两个作用:一是吸收多余的氯气,另一个是防止空气中水蒸气进入.
(4)工业上以硫黄、液氯和液体三氧化硫为原料,能生产高纯度(99%以上)氯化亚砜,为使三种原料恰好完全反应,三者的物质的量比为1:1:1.
分析 装置A制备氯气,装置B吸收氯气的中HCl,装置C干燥氯气,D装置生成SCl2,E装置收集SCl2,F装置吸收多余的氯气,吸收空气中水蒸气,防止进入E中,
(1)制备气体,装置气密性要好;加热硫粉时,空气中的氧气能与硫粉反应;
(2)用饱和氯化钠溶液吸收HCl;由仪器5的特征,可知为蒸馏烧瓶;增大反应物接触面积;
(3)二氯化硫(SCl2)的沸点低,易挥发,可以用冰水冷却;防止空气中水蒸气进入;
(4)根据方程式判断硫黄、液氯和液体三氧化硫的物质的量之比;
解答 解:装置A制备氯气,装置B吸收氯气的中HCl,装置C干燥氯气,D装置生成SCl2,E装置收集SCl2,F装置吸收多余的氯气,吸收空气中水蒸气,防止进入E中.
(1)仪器组装完成后,首先进行的一步操作是:检查装置气密性;加热硫粉时,空气中的氧气与硫粉反应,应先排尽系统中空气,
故答案为:检查装置气密性;防止加热硫粉时,空气中的氧气与硫粉反应;
(2)B装置吸收氯气中的HCl,用饱和氯化钠溶液反应吸收;由仪器5的特征,可知为蒸馏烧瓶,
故答案为:饱和氯化钠溶液;蒸馏烧瓶;
(3)二氯化硫(SCl2)的沸点低,为防止SCl2中液体挥发,可采取将锥形瓶放入冰水中冷却等措施,装置F(盛放碱石灰)有两个作用:一是吸收多余的氯气,另一个是:防止空气中水蒸气进入,
故答案为:将锥形瓶放入冰水中冷却;防止空气中水蒸气进入;
(4)由S(s)+Cl2(g)$\frac{\underline{\;\;△\;\;}}{\;}$SCl2(l)、SCl2(l)+SO3(l)═SOCl2(l)+SO2(g)可知硫黄、液氯和液体三氧化硫的物质的量之比为1:1:1,
故答案为:1:1:1.
点评 本题考查化学实验制备方案,涉及基本操作、对操作与装置的分析评价、物质检验等,较好的考查学生对知识的迁移运用能力,难度中等.

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案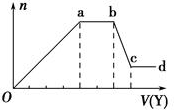 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
(1)若Y是盐酸,则X溶液中一定含有的离子是SiO32-、AlO2-、CO32-、Na+,ab段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑,图中Oa段与Y溶液反应的离子的物质的量之比为【要标明离子符号,如n(Na+)】.
(2)若Y是NaOH溶液,则ab段反应的离子方程式为NH4++OH-═NH3•H2O; bc段反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.若不考虑离子的水解因素,忽略H+和OH-,且溶液中只存在4种离子,则它们的离子个数比为【要标明离子符号,如n(Na+),按阳离子在前,阴离子在后,高价在前,低价在后得顺序排列】.
| A. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | B. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | ||
| C. | 2HCl+Zn═ZnCl2+H2↑ | D. | NaCl+AgNO3═AgCl↓+NaNO3 |
| A. |  用图所示装置氧化Br- | |
| B. | 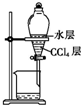 用图所示装置萃取Br2 | |
| C. | 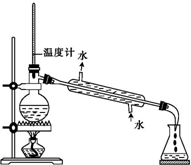 用图所示装置分离CCl4和Br2 | |
| D. | 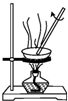 用图所示的装置将含AlCl3的溶液蒸发制取无水AlCl3 |
| A. | 2.1 g | B. | 3.6 g | C. | 7.2 g | D. | 无法确定 |
 能源问题是当前人类社会面临的一项重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为285.8kJ/mol、282.5kJ/mol、726.7kJ/mol.请回答:
能源问题是当前人类社会面临的一项重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为285.8kJ/mol、282.5kJ/mol、726.7kJ/mol.请回答: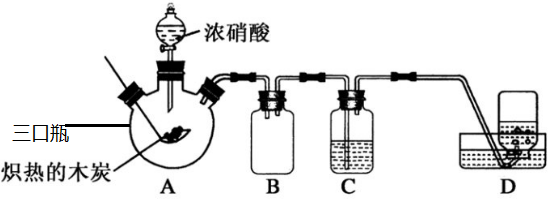
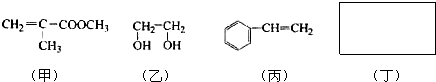
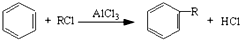
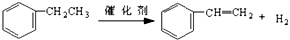
 .
. .
.