题目内容
【题目】右图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
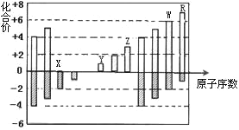
A. 原子半径:Z>Y>X
B. 气态氢化物的还原性: R < W
C. WX3和水反应形成的化合物是共价化合物
D. 含Z的两种盐溶液反应的离子方程式是Z3++ZO2-+H2O=2Z(OH)3↓
【答案】C
【解析】
为短周期元素,有两种元素既有+4价,又有-4价,故前一种元素为碳,后一种元素为硅,故R为Si元素,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,据此分析作答。
根据上述分析可知,X、Y、Z、W和R分别是O、Na、Al、S和Si,则
A. 同周期随原子序数增大,原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>O,即Y>Z>X,A项错误;
B.非金属性S>Si,则氧化性:S>Si;气态氢化物的还原性:S<Si,B项错误;
C.SO3与H2O化合生成H2SO4,H2SO4是共价化合物,C项正确;
D.含Z的两种盐溶液分别是铝离子与偏铝酸根离子,其反应的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓,D项错误;
答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】已知X、Y、Z、M、R五种元素中,原子序数依次增大,其结构或性质信息如下表。请根据信息回答有关问题:
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 在元素周期表的各元素中电负性仅小于氟 |
M | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子 |
R | 第四周期过渡元素,其价电子层各能级处于半充满状态 |
(1)元素M的原子核外有 ______ 种不同运动状态的电子;
(2)五种元素中第一电离能最高的是_______写元素符号;
(3)在Y形成的单质中,![]() 键与
键与![]() 键数目之比为______,在
键数目之比为______,在![]() 中Z原子的杂化方式为_____,其分子的空间构型为 ______;
中Z原子的杂化方式为_____,其分子的空间构型为 ______;
(4)R的一种配合物的化学式为![]() 。已知
。已知![]() 在水溶液中用过量硝酸银溶液处理,产生
在水溶液中用过量硝酸银溶液处理,产生![]() AgCl沉淀,此配合物最可能是 ______填序号。
AgCl沉淀,此配合物最可能是 ______填序号。
A.![]() B.
B.![]()
C.![]() D.
D.![]()