题目内容
【题目】已知X、Y、Z、M、R五种元素中,原子序数依次增大,其结构或性质信息如下表。请根据信息回答有关问题:
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 在元素周期表的各元素中电负性仅小于氟 |
M | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子 |
R | 第四周期过渡元素,其价电子层各能级处于半充满状态 |
(1)元素M的原子核外有 ______ 种不同运动状态的电子;
(2)五种元素中第一电离能最高的是_______写元素符号;
(3)在Y形成的单质中,![]() 键与
键与![]() 键数目之比为______,在
键数目之比为______,在![]() 中Z原子的杂化方式为_____,其分子的空间构型为 ______;
中Z原子的杂化方式为_____,其分子的空间构型为 ______;
(4)R的一种配合物的化学式为![]() 。已知
。已知![]() 在水溶液中用过量硝酸银溶液处理,产生
在水溶液中用过量硝酸银溶液处理,产生![]() AgCl沉淀,此配合物最可能是 ______填序号。
AgCl沉淀,此配合物最可能是 ______填序号。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
【答案】 17 N 1:2 ![]() V型 B
V型 B
【解析】
已知X、Y、Z、M、R五种元素中,原子序数X<Y<Z<M<R,X元素原子原子的L层上s电子数等于p电子数,核外电子排布为![]() ,则X为C元素;Y元素原子核外的L层有3个未成对电子,核外电子排布为
,则X为C元素;Y元素原子核外的L层有3个未成对电子,核外电子排布为![]() ,则Y为N元素;Z元素在元素周期表的各元素中电负性仅小于氟,则Z为O元素;M元素单质常温、常压下是气体,原子的M层上有1个未成对的p电子,原子核外电子排布为
,则Y为N元素;Z元素在元素周期表的各元素中电负性仅小于氟,则Z为O元素;M元素单质常温、常压下是气体,原子的M层上有1个未成对的p电子,原子核外电子排布为![]() ,则M为Cl;第四周期过渡元素,其价电子层各能级处于半充满状态,应为Cr元素,价层电子排布式为
,则M为Cl;第四周期过渡元素,其价电子层各能级处于半充满状态,应为Cr元素,价层电子排布式为![]() 。
。
(1)M为Cl,原子核外电子排布为![]() 共有17种不同运动状态的电子,有5种不同能级的电子;
共有17种不同运动状态的电子,有5种不同能级的电子;
(2)同一主族元素的第一电离能随着原子序数的增大而减小,同一周期元素的第一电离能随着原子序数的增大而增大,注意同一周期的第ⅡA元素的第一电离能大于第ⅢA族的,第ⅤA族的大于第ⅥA族的,因为N原子的2p能级电子为半充满,为较稳定的结构,则N的第一电能较大;
(3)根据题意知Y的单质为N2,其中氮氮之间存在1个![]() 键和2个
键和2个![]() 键,因此
键,因此![]() 键与
键与![]() 键数目之比为1:2。
键数目之比为1:2。![]() 中心氧原子有6个价电子,两个Cl分别提供一个电子,所以中心原子价电子对数
中心氧原子有6个价电子,两个Cl分别提供一个电子,所以中心原子价电子对数![]() ,中心O原子杂化为
,中心O原子杂化为![]() 杂化,空间构型为V型;
杂化,空间构型为V型;

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案【题目】采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为___________。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
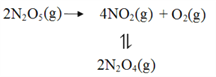
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O4(g)完全分解):
t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
p/kPa | 35.8 | 40.3 | 42.5. | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=4.4 kJ·mol1
2NO2(g)=N2O4(g) ΔH 2=55.3 kJ·mol1
则反应N2O5(g)=2NO2(g)+ ![]() O2(g)的ΔH=_______ kJ·mol1。
O2(g)的ΔH=_______ kJ·mol1。
②研究表明,N2O5(g)分解的反应速率![]() 。t=62 min时,测得体系中
。t=62 min时,测得体系中![]() pO2=2.9 kPa,则此时的
pO2=2.9 kPa,则此时的![]() =________kPa,v=_______kPa·min1。
=________kPa,v=_______kPa·min1。
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____63.1 kPa(填“大于”“等于”或“小于”),原因是________。
④25℃时N2O4(g)![]() 2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5![]() NO2+NO3 快速平衡
NO2+NO3 快速平衡
第二步 NO2+NO3→NO+NO2+O2 慢反应
第三步 NO+NO3→2NO2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______(填标号)。
A.v(第一步的逆反应)>v(第二步反应)
B.反应的中间产物只有NO3
C.第二步中NO2与NO3的碰撞仅部分有效
D.第三步反应活化能较高
【题目】某工业流程中,进入反应塔的混合气体中NO和O2的物质的量分数分别为0.10和0.06,发生化学反应2NO(g)+O2(g)=2NO2(g),在其他条件相同时,测得实验数据如下表:
压强/(×105Pa) | 温度/℃ | NO达到所列转化率需要时间/s | ||
50% | 90% | 98% | ||
1.0 | 30 | 12 | 250 | 2830 |
90 | 25 | 510 | 5760 | |
8.0 | 30 | 0.2 | 3.9 | 36 |
90 | 0.6 | 7.9 | 74 | |
根据表中数据,下列说法正确的是
A. 升高温度,反应速率加快
B. 增大压强,反应速率变慢
C. 在1.0×105Pa、90℃条件下,当转化率为98%时的反应已达到平衡
D. 若进入反应塔的混合气体为amol,反应速率以v=△n/△t表示,则在8.0×105Pa、30℃条件下转化率从50%增至90%时段NO的反应速率为4a/370mol/s