题目内容
10.根据下列操作及现象,所得结论正确的是( )| 序号 | 操作及现象 | 结论 |
| A | 向2mL1mol/LNaOH溶液中先加入3滴1mol/LMgCl2溶液,再加入3滴1mol/LFeCl3 | Mg(OH)2转化为Fe(OH)3 |
| B | 常温下,测得饱和Na2CO3溶液的pH大于饱和NaHCO3溶液 | 常温下水解程度:CO32->HCO3- |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 溴乙烷与NaOH乙醇溶液共热产生的气体通入KMnO4酸性溶液中,溶液褪色 | 产生的气体为乙烯 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NaOH溶液体积未知,可能过量,不能说明沉淀转化;
B.Na2CO3溶解度较大,应比较相同的浓度的溶液的pH;
C.盐类的水解为吸热反应,升高温度促进水解;
D.不能排除乙醇的影响.
解答 解:A.NaOH溶液体积未知,可能过量,不能说明沉淀转化,过量NaOH与氯化铁反应生成Fe(OH)3沉淀,故A错误;
B.饱和溶液的浓度不同,Na2CO3溶解度较大,应比较相同的浓度的溶液的pH,故B错误;
C.盐类的水解为吸热反应,升高温度促进水解,可根据溶液颜色判断,故C正确;
D.乙醇易挥发,且能与酸性高锰酸钾发生氧化还原反应,不能排除乙醇的影响,应先通过水,除去乙醇,故D错误.
故选C.
点评 本题考查较为综合,涉及沉淀的转化、盐类的水解、物质的检验,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的合理性和可行性的评价,难度不大.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
20.下列叙述正确的是( )
| A. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O互称同素异形体 | B. | 丙烷和异丁烷互称同系物 | ||
| C. | 金刚石和石墨互称同位素 | D. |  和 和 互称同分异构体 互称同分异构体 |
1.一定条件下合成乙烯:6H2(g)+2CO2(g)$\stackrel{催化剂}{?}$CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( )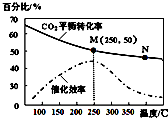

| A. | 生成乙烯的速率:v(M)有可能小于v(N) | |
| B. | 平衡常数:KM>KN | |
| C. | 当温度高于250℃,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低 | |
| D. | 若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7% |
18.在溶液中能大量共存的一组离子或分子是( )
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、Al3+、SO42-、NH3•H2O | ||
| C. | Na+、K+、SO32-、Cl2 | D. | Na+、Mg2-、SO42-、H+ |
5.根据元素性质周期表递变规律,下列判断均正确的是( )
| A. | 酸性:HClO4>HBrO4>HIO4 碱性:NaOH>KOH>RbOH | |
| B. | 原子半径:Na>O>F 离子半径::Na+>O2->F- | |
| C. | 稳定性::HF>H2O>H2S 还原性:HCl<H2S<PH3 | |
| D. | 还原性:Na>Mg>Al 氧化性:P>S>Cl2 |
15.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 饱和氯水中:Cl-、NO3-、Na+、CO32- | |
| B. | c(H+)=1.0×10-13mol•L的溶液中:MnO4-、K+、SO42-、AlO2- | |
| C. | c(AlO2-)=1.0mol•L的溶液中:SO42-、K+、Cl-、HCO3- | |
| D. | pH=7的溶液中:NO2-、I-、Na+、Fe3+ |
2.下列反应的能量变化情况符合如图的是( )
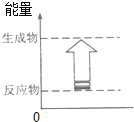

| A. | 石灰石在高温下的分解反应 | B. | 金属钠和水的反应 | ||
| C. | 盐酸与氢氧化钠溶液的反应 | D. | 木炭在氧气中燃烧 |
19.下列叙述正确的是( )
| A. | 纤维素和淀粉互称同分异构体 | B. | 甲烷和异丁烷互称同系物 | ||
| C. | 金刚石和石墨互称同位素 | D. |  和 和 互称同分异构体 互称同分异构体 |