��Ŀ����
��һ���¶Ⱥ�ѹǿ�£���ʢ������X������ɱ���ܱ�������ͨ��Y���壬������Ӧ�� X(s)+aY(g) bZ(s)+W(g)����H>0
bZ(s)+W(g)����H>0
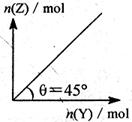
ƽ��ʱZ�����ʵ�����ͨ��Y�����ʵ����ı仯��ϵ��ͼ��ʾ������˵������ȷ����( ��
 bZ(s)+W(g)����H>0
bZ(s)+W(g)����H>0ƽ��ʱZ�����ʵ�����ͨ��Y�����ʵ����ı仯��ϵ��ͼ��ʾ������˵������ȷ����( ��

| A��ƽ��ʱY��ת����Ϊ(a/b)% |
| B�����������ټ�������X����Y��ת�������� |
| C����ͨ��Y�����´ﵽƽ��ʱW������������� |
| D������ѹǿһ������ԭ��Ӧ�ڽϸ��¶��½���ƽ��ʱ��ͼ�Ц�<450 |
C
����ͼ���б�ʿ��жϣ�ÿ����1molY����Ӧ������1molZ����a��b��A����ȷ��X�ǹ��壬����X����Ӱ��ƽ��״̬��B����ȷ����Ϊ�Ǻ��º�ѹ���ҷ�Ӧ����������ֻ��һ�����壬���Ըı�Y�����ʵ�����ƽ�ⲻ�ƶ���C��ȷ����Ӧ�����ȷ�Ӧ���¶ȸߣ���Ӧ���ת���ʴ�Y��Z�ı仯��֮���ǹ���ģ����ԽǶȲ��䣬D����ȷ����ѡC��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����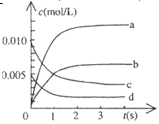
 Ur������������ӣ���H3O�� Ur��(��Һ)��Na������Һ��
Ur������������ӣ���H3O�� Ur��(��Һ)��Na������Һ�� 2NH3(g) Ϊ���ȷ�Ӧ��400�� 30 MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ����
2NH3(g) Ϊ���ȷ�Ӧ��400�� 30 MPa��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ���� Cr(OH)3(����ɫ)
Cr(OH)3(����ɫ)  2C��g���ﵽƽ��ı�־���ǣ� ��
2C��g���ﵽƽ��ı�־���ǣ� ��  PCl3��g��+Cl2��g������ƽ������������г���amol PCl5���ٴδﵽƽ�����ԭƽ��Ƚϣ�������������ȷ���� �� ��
PCl3��g��+Cl2��g������ƽ������������г���amol PCl5���ٴδﵽƽ�����ԭƽ��Ƚϣ�������������ȷ���� �� ��