题目内容
(7分)在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2?2NH3已知加入1 mol N2、4 mol H2时,达到平衡后生成a mol NH3(见表中已知项),在相同温度和压强下保持平衡后各组分体积分数不变,对下列编号①~③的状态,填写表中空白。
| 已知编号 | 始态的物质的量(mol) | 平衡时NH3的 物质的量(mol) | ||
| N2 | H2 | NH3 | ||
| 已知 | 1 | 4 | 0 | a |
| ① | | | 1 | 0.5a |
| ② | 1.5 | 6 | 0 | |
| ③ | m | n( n≥4m) | | |
① n (N2)="0" (1分) n (H2)="0.5" (1分) ② n(NH3)="1.5a" (1分)
③始态NH3为:2(n-4m) (2分) 平衡时NH3为(n-3m)a (2分)
③始态NH3为:2(n-4m) (2分) 平衡时NH3为(n-3m)a (2分)
(1)在保持恒压时要使平衡等效,则最初的投料的比值是相同的,根据题意可知最初的氮气和氢气的体积之比是1︰4的,所以通过方程式换算后的氮气和氢气的体积之比必须满足1︰4。在实验③中设氨气的物质的量是x,则xmol氨气可以生成0.5xmol氮气和1.5xmol氢气,则一定有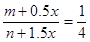 ,解得x=2(n-4m)mol。平衡是等效的,所以各种物质的含量分别是相同的,所以平衡时氨气的物质的量是不同的。氨气的物质的量和起始时氮气的物质的量成正比。
,解得x=2(n-4m)mol。平衡是等效的,所以各种物质的含量分别是相同的,所以平衡时氨气的物质的量是不同的。氨气的物质的量和起始时氮气的物质的量成正比。
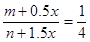 ,解得x=2(n-4m)mol。平衡是等效的,所以各种物质的含量分别是相同的,所以平衡时氨气的物质的量是不同的。氨气的物质的量和起始时氮气的物质的量成正比。
,解得x=2(n-4m)mol。平衡是等效的,所以各种物质的含量分别是相同的,所以平衡时氨气的物质的量是不同的。氨气的物质的量和起始时氮气的物质的量成正比。
练习册系列答案
相关题目
 C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )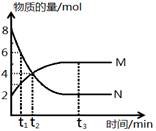
 N
N WI2(g)ΔH<0
WI2(g)ΔH<0
 bZ(s)+W(g);△H>0
bZ(s)+W(g);△H>0
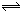 F(g)+xG(g) △H<0,若起始时E的浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5 a mol/L;若E的起始浓度改为2 a mol/L,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是( )
F(g)+xG(g) △H<0,若起始时E的浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5 a mol/L;若E的起始浓度改为2 a mol/L,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是( )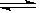 2NH3(g)不能作为达到平衡状态的依据的是
2NH3(g)不能作为达到平衡状态的依据的是 3C(g )+D(g ),若反应开始时充入2 molA和1 molB,达到平衡时C的物质的量浓度为amol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的物质的量的浓度仍然为amol/L的是( )
3C(g )+D(g ),若反应开始时充入2 molA和1 molB,达到平衡时C的物质的量浓度为amol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的物质的量的浓度仍然为amol/L的是( )