题目内容
【化学—选修3:物质结构与性质】(15分)
氮化钛( Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金代替品。以TiCl4为原料,经过一系列反应(如图所示),可以制得Ti3N4和纳米TiO2请回答下列问题:

(1)反应①为置换反应,写出该反应的化学方程式 ;TiCl4分子中4个氯原子不在同一平面上,则TiCl4的空间构型为 。
(2)元素周期表中Ti元素位于第 周期 族。与Ti相邻的元素Zr的基态原子外围电子排布式为 ,
(3)纳米TiO2是一种应用广泛的催化剂,纳米Ti02催化的一个实验如图所示。

化合物甲的分子中采取sp2方式杂化的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。
(4)有一种氮化钛晶体的晶胞如图所示,该氮化钛晶胞中含有 个N原子,晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为 g.cm-3(NA为阿伏加德常数的数值,只列算式)。

氮化钛( Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金代替品。以TiCl4为原料,经过一系列反应(如图所示),可以制得Ti3N4和纳米TiO2请回答下列问题:

(1)反应①为置换反应,写出该反应的化学方程式 ;TiCl4分子中4个氯原子不在同一平面上,则TiCl4的空间构型为 。
(2)元素周期表中Ti元素位于第 周期 族。与Ti相邻的元素Zr的基态原子外围电子排布式为 ,
(3)纳米TiO2是一种应用广泛的催化剂,纳米Ti02催化的一个实验如图所示。

化合物甲的分子中采取sp2方式杂化的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。
(4)有一种氮化钛晶体的晶胞如图所示,该氮化钛晶胞中含有 个N原子,晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为 g.cm-3(NA为阿伏加德常数的数值,只列算式)。

(除第(2)题每空1分,其余每空2分,共15分)
(1)2Mg+TiCl4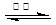 Ti+MgCl2 正四面体
Ti+MgCl2 正四面体
(2)四、IVB 4d25S2
(3)7 N>O>C
(4)4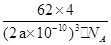
(1)2Mg+TiCl4
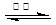 Ti+MgCl2 正四面体
Ti+MgCl2 正四面体(2)四、IVB 4d25S2
(3)7 N>O>C
(4)4
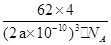
试题分析:(1)反应①为置换反应,镁置换钛,所以化学方程式为2Mg+TiCl4
 Ti+MgCl2 ;TiCl4的价层电子对数="4+1/2(4-4×1)=4," TiCl4分子中4个氯原子不在同一平面上,所以TiCl4的空间构型为正四面体型;
Ti+MgCl2 ;TiCl4的价层电子对数="4+1/2(4-4×1)=4," TiCl4分子中4个氯原子不在同一平面上,所以TiCl4的空间构型为正四面体型;(2)元素周期表中Ti元素位于第四周期第IVB族,Zr与Ti同族,在Ti的下一周期,所以外围电子排布式与Ti相似,为4d25s2
(3)采取sp2方式杂化的碳原子周围有3个共价单键,所以甲中的苯环中有6个,-C=O中的1个,共7 个sp2方式杂化的碳原子;根据杂化轨道的判断方法,化合物乙中采取sp3杂化的原子,包括C原子,羟基中的O原子和氨基的N原子,N原子的2p轨道为半充满状态,所以第一电离能最大,C原子的第一电离能最小,所以三者的第一电离能由大到小的顺序为N>O>C;
(4)N原子位于立方体的8个顶点和6个面的面心位置,所以晶胞中N原子的个数=8×1/8+6×1/2=4个;Ti原子位于12条棱的中点和立方体的中心,所以晶胞中Ti原子的个数=12×1/4+1=4个;晶胞中N、Ti之间的最近距离为a pm,则晶胞的棱长为2apm=2a×10-10cm,则该氮化钛的密度为4×62/NA/(2a×10-10)3=
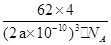 g.cm-3
g.cm-3
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
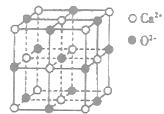
 ,下列有关说法正确的是________(填选项字母)。
,下列有关说法正确的是________(填选项字母)。
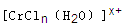 (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应: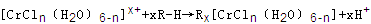
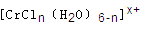 的溶液,与R-H完全交换后,中和生成的需浓度为
的溶液,与R-H完全交换后,中和生成的需浓度为 键的数目为____ __________________.
键的数目为____ __________________. g/cm
g/cm ,阿伏加德罗常数为
,阿伏加德罗常数为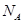 ,求晶胞边长a=________cm。(用含
,求晶胞边长a=________cm。(用含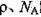 的计算式表示)
的计算式表示)
 和黑色的HD两种化合物。
和黑色的HD两种化合物。 中B原子采取的杂化轨道类型为 。
中B原子采取的杂化轨道类型为 。 分子的空间构型为 。
分子的空间构型为 。 极易溶于
极易溶于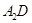 ,原因是 。
,原因是 。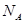 表示阿伏伽德罗常数,晶胞的边长为a。晶胞的高为h,则晶胞的密度可表示为 g/cm3。(用只含r和
表示阿伏伽德罗常数,晶胞的边长为a。晶胞的高为h,则晶胞的密度可表示为 g/cm3。(用只含r和


 键有________mol。
键有________mol。
