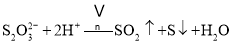题目内容
【题目】下列说法正确的是( )
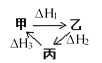
A.甲、乙、丙三物质转化如图所示,则![]()
B.1molCO完全燃烧生成稳定氧化物放出热量为![]() ,则2
,则2 ![]()
![]() ,
,![]()
C.若![]() ,
,![]() ,故在某容器中充入
,故在某容器中充入![]() 与
与![]() 充分反应后,放出的热量为
充分反应后,放出的热量为![]()
D.常温下,稀HCl和稀NaOH溶液反应生成![]() 放出热量为
放出热量为![]() ,其热化学方程式为
,其热化学方程式为![]() ,
,![]()
【答案】B
【解析】
![]() 根据图示及盖斯定律可得:
根据图示及盖斯定律可得:![]() ,故A错误;
,故A错误;
B.1molCO完全燃烧生成稳定氧化物放出热量为![]() ,则2mol二氧化碳分解生成2molCO和氧气吸收566kJ的热量,该反应的热化学方程式为:
,则2mol二氧化碳分解生成2molCO和氧气吸收566kJ的热量,该反应的热化学方程式为:![]() ,
,![]() ,故B正确;
,故B正确;
C.若![]() ,
,![]() ,说明生成2mol氨气放出
,说明生成2mol氨气放出![]() 的热量,由于合成氨为可逆反应,则在某容器中充入
的热量,由于合成氨为可逆反应,则在某容器中充入![]() 与
与![]() 充分反应后,生成的氨气小于2mol,所以放出的热量小于
充分反应后,生成的氨气小于2mol,所以放出的热量小于![]() ,故C错误;
,故C错误;
D.常温下,稀HCl和稀NaOH溶液反应生成![]() 放出热量为
放出热量为![]() ,正确的热化学方程式为:
,正确的热化学方程式为:![]() ,
,![]() ,故D错误;
,故D错误;
答案选B。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】部分难溶物的颜色和常温下的Ksp如下表所示:
Cu(OH)2 | CuOH | CuCl | Cu2O | |
颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
Ksp(25 ℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | — |
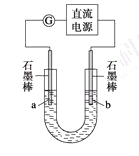
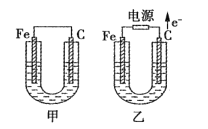
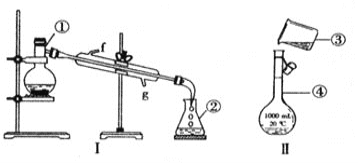
某研究性学习小组对电解食盐水进行了如下探究:
实验Ⅰ装置如图所示,接通电源后,发现a、b电极上均有气泡产生。
(1)电解过程中的总离子反应方程式为_________________________________________。
(2)为了确定电源的正、负极,下列操作一定行之有效的是_______。
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示。
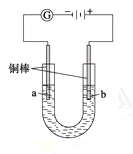
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5 min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10 min后,最靠近a极的白色沉淀开始变成红色;
④12 min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色。
(3) a极发生的电极反应方程式为________________________________________________________。
(4) 电解5 min后,b极发生的电极反应方程式为___________________________________________。
(5)12 min后,b极附近出现的橙黄色沉淀的成分是_____,原因是___________________________________________________________________________________。