题目内容
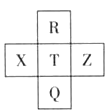
【题目】元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是( )
A. T的单质在化学反应中只表现氧化性
B. R与Q的电子数相差16
C. T形成的含氧酸的酸性一定比X形成的含氧酸强
D. 在这五种元素中Z的化学性质最稳定
【答案】D
【解析】R单质在暗处与氢气剧烈化合并发生爆炸,因此R为F,T为Cl,Q为Br,X为S,Z为Ar,A、Cl2和NaOH反应:Cl2+2NaOH=NaCl+NaClO+H2O,氯气既作氧化剂又作还原剂,故A错误;B、R与Q电子数相差(35-9)=26,故B错误;C、Cl形成含氧酸是HClO和HClO4,X的含氧酸是H2SO3和H2SO4,HClO属于弱酸,酸性小于H2SO4,故C错误;D、Z为稀有气体,化学性质最稳定,故D正确。

【题目】化学反应速率与限度与生产、生活密切相关
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①反应速率最大的时间段是(指0~1、1~2、2~3、3~4、4~5 )____min,原因是_________________。
②求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率________________。(设溶液体积不变)
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列__________以减慢反应速率。(填写代号)
A.蒸馏水 B.冰块 C.HNO3溶液 D.CuSO4溶液
(3)某温度下在10L密闭容器中,3种气态物质A、B、C的物质的量随时间变化曲线如图。

①该反应的化学方程式是________。
②求在该条件达到反应的限度(平衡状态)时反应物的转化率【转化率=(转化的物质的量/初始物质的量)×100%】,请写出计算过程,计算结果保留1位小数)________