题目内容
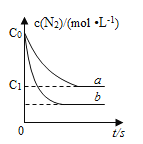
【题目】汽车尾气中,产生NO的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
A.温度T下,该反应的平衡常数K=![]()
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
【答案】A
【解析】A、由平衡常数的计算公式得K=![]() ,又因为氮气和氧气的物质的量相同,所以A正确;B、由于反应在恒容的密闭容器中反应,所以气体总体积保持不变,且质量守恒,所以混合气体密度的不变,故B错误;C、催化剂只能改变反应速率,不能改变化学反应限度,而图中显示平衡时氮气的浓度发生了变化,故C错误;D、若曲线b对应的条件改变是温度,却不知道是升高还是降低温度,所以无法推测△H,故D错误;此题选A。
,又因为氮气和氧气的物质的量相同,所以A正确;B、由于反应在恒容的密闭容器中反应,所以气体总体积保持不变,且质量守恒,所以混合气体密度的不变,故B错误;C、催化剂只能改变反应速率,不能改变化学反应限度,而图中显示平衡时氮气的浓度发生了变化,故C错误;D、若曲线b对应的条件改变是温度,却不知道是升高还是降低温度,所以无法推测△H,故D错误;此题选A。

练习册系列答案
相关题目