题目内容
(10分) 按下列要求回答:现有: ①BaCl2;②冰;③NH4Cl;④Na2SO4;⑤干冰;⑥碘片 六种物质。
(1) 属于离子化合物的是__________(填序号,下同),物质中只有离子键的物质有________,
属于共价化合物的是________。
(2) 熔化时不需要破坏化学键的是__________,熔点最低的是__________。
(1) ①③④ ① ②⑤ (2) ②⑤⑥ ⑤
解析试题分析:(1)离子化合物中含有离子键,①BaCl2③NH4Cl④Na2SO4三种化合物中含有离子键,而③NH4Cl④Na2SO4这两种化合物中除了含有离子键外还有共价键;在共价化合物中只有共价键,②冰⑤干冰中只有共价键,属于共价化合物。
(2)②冰⑤干冰⑥碘片三种物质溶于水是不需要破坏化学键;熔点最低的是分子晶体,在分子晶体中,熔点最低的是分子间作用力最小的,故为⑤干冰。
考点:离子键与共价键化学键和离子化合物与共价化合物的关系

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列观点正确的是( )
| A.构成单质分子的微粒一定含有共价键 |
| B.在氧化钠中,只存在氧离子和钠离子的静电吸引作用 |
| C.某化合物熔融态能导电,该化合物中一定有离子键 |
| D.Na2O和Na2O2所含化学键类型完全相同 |
下列说法正确的是
| A.全部由非金属元素组成的化合物一定是共价化合物 |
| B.含有共价键的化合物不一定是共价化合物 |
| C.由共价键形成的分子一定是共价化合物 |
| D.硫酸分子中有H+和SO42-两种离子 |
配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是
| A.CO2 | B.H3O+ | C.CH4 | D.[Ag(NH3)2] + |
(3)配位化学创始人维尔纳发现,将各为1mol的CoCl3·6NH3(黄色)、CoCl3·5NH3(紫红色)、CoCl3·4NH3(绿色)、CoCl3·4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为3mol、2mol、1mol、和1mol。已知上述配合物中配离子的配位数均为6。请根据实验事实用配合物的形式写出它们的化学式。
①CoCl3·5NH3 ②CoCl3·4NH3(紫色)
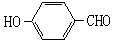 和
和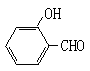 的沸点高低并说明理由_________。
的沸点高低并说明理由_________。 从海水得到的无水MgC12中提取金属镁
从海水得到的无水MgC12中提取金属镁 的单体有 ______________________________
的单体有 ______________________________