题目内容
10.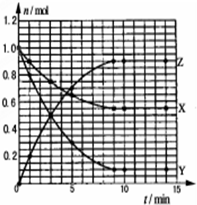 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )| A. | 反应的化学方程式是X+2Y?2Z | |
| B. | 该反应在0-3min时间内产物Z的平均反应速率0.083mol•L-1•min-1 | |
| C. | 由图象知该反应吸收能量 | |
| D. | 其他条件不变,升高温度,若正反应速率增大,则逆反应速率将减小 |
分析 A、依据图象计算达到平衡状态各物质的物质的量变化,物质的量变化之比等于化学方程式计量数之比,据此写出化学方程式;
B、反应速率V=△c△t△c△t计算得到;
C、图象是物质在反应过程中物质的量的变化曲线,不能判断反应热量变化;
D、升高温度增大反应速率,正逆反应速率都增大.
解答 解:A、依据图象计算达到平衡状态各物质的物质的量变化,物质的量变化之比等于化学方程式计量数之比,物质的量变化分析XY为反应物,Z为生成物,物质的量变化之比为,n(X):n(Y):n(Z)=(1.0mol-0.55mol):(1.0mol-0.1mol):0.9mol=1:2:2,据此写出化学方程式为X+2Y?2Z,故A正确;
B、反应速率V=△c△t△c△t,该反应在0-3min时间内产物Z的平均反应速率=0.5mol2L3min0.5mol2L3min=0.083mol•L-1•min-1,故B正确;
C、图象只是反应物和生成物物质的量变化趋势,不能表达反应随温度的变化,故C错误;
D、升高温度增大反应速率,正逆反应速率都增大,只是增大程度不同,故D错误;
故选CD.
点评 本题考查了化学图象的分析判断,化学反应速率、转化率概念的计算分析,主要是化学方程式书写方法和影响反应速率因素的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
5.常温下,在下列指定条件的各溶液中,一定能大量共存的离子组是( )
| A. | 含0.1 mol/L-1SO2的溶液中:Na+、Ba2+、Br-、Cl- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Mg2+、NO3-、SO42- | |
| C. | 碱性溶液中:K+、NH4+、SO42-、NO3- | |
| D. | 不能使酚酞变红的无色溶液中:Na+、K+、MnO4-、I- |
6.短周期主族元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.Z原子的最外层电子数是X原子内层电子数的3倍,也是Y原子最外层电子数的3倍.X与Y、Z位于相邻的周期.下列说法正确的是( )
| A. | X的最高价氧化物对应的水化物是弱酸 | |
| B. | 元素Z位于元素周期表的第3周期Ⅵ族 | |
| C. | Y形成的单质能在二氧化碳中燃烧 | |
| D. | 原子半径的大小顺序:r(Z)>r(Y)>r(X) |
3.已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15,在存在AB2、AC固定的饱和的混合溶液中,测得c(C2-)=1.8×10-13 mol/L,则下列说法正确的是( )
| A. | 溶液中c(B-)为1.6×10-3mol/L | |
| B. | 溶液中c(B-)为1.7×10-13mol/L | |
| C. | AB2比AC更难溶解 | |
| D. | 因两者不同类而无法比较其溶解度的大小 |
5.能正确表示下列反应的方程式的是( )
| A. | 用铜电极电解饱和氯化钠溶液:2Cl-+2H2O电解_2OH-+H2↑+Cl2↑ | |
| B. | 过量铁与氯气反应:2Fe+3Cl2△_2FeCl3 | |
| C. | 过氧化钠与水反应:2O22-+2H2O=4OH-+O2↑ | |
| D. | 向石灰水中滴加少量Ca(HCO3)2溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
15.下列化学式能真实表示该物质分子的是( )
| A. | 硫酸(H2SO4) | B. | 铁(Fe) | C. | 红磷(P) | D. | 氮化硼(BN) |
2.在100kPa下,12g石墨完全转化为金刚石需要吸收1.895kJ的热能.据此在100kPa时,下列说法正确的是( )
| A. | 石墨转化为金刚石不是化学变化 | |
| B. | 金刚石比石墨稳定 | |
| C. | 1mol石墨具有的总能量比1mol金刚石的低 | |
| D. | 等质量的石墨与金刚石完全燃烧,石墨放出的能量多 |
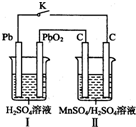 锰及其化合物应用越来越广泛,MnO2是一种重要的无机功能材料,制备MnO2的方法之一是以石墨为电极,电解酸化的MnSO4溶液,阳极的电极反应式为Mn2+-2e-+2H20=MnO2+4H+.
锰及其化合物应用越来越广泛,MnO2是一种重要的无机功能材料,制备MnO2的方法之一是以石墨为电极,电解酸化的MnSO4溶液,阳极的电极反应式为Mn2+-2e-+2H20=MnO2+4H+.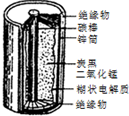 某学校设计了一节实验活动课,让学生从废旧的锌锰酸性干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个实验过程如下,请回答有关问题:
某学校设计了一节实验活动课,让学生从废旧的锌锰酸性干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个实验过程如下,请回答有关问题: