题目内容
3.已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15,在存在AB2、AC固定的饱和的混合溶液中,测得c(C2-)=1.8×10-13 mol/L,则下列说法正确的是( )| A. | 溶液中c(B-)为1.6×10-3mol/L | |
| B. | 溶液中c(B-)为1.7×10-13mol/L | |
| C. | AB2比AC更难溶解 | |
| D. | 因两者不同类而无法比较其溶解度的大小 |
分析 AB、依据Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15,分别列出其表达式,利用c(C2-)=1.8×10-13 mol/L计算即可;
CD、AB2、AC两者Ksp(AB2)=c(A2+)×c2(B-),Ksp(AC)=c(A2+)×c(C2-),两者不类似,不能比较溶解度的大小.
解答 解:A、已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15.在AB2、AC均为饱和的混合液中,Ksp(AB2)=c(A2+)×c2(B-)=4.2×10-8,Ksp(AC)=c(A2+)×c(C2-)=3.0×10-15.得到,Ksp(AB2):Ksp(AC)=c(A2+)×c2(B-):c(A2+)×c(C2-)=4.2×10-8:3.0×10-15 测得c(C2-)=1.8×10-13 mol•L-1,则c(B-)=1.6×10-3 mol/L,故A正确;
B、依据A的计算c(B-)=1.6×10-3 mol/L,故B错误;
C、AB2与AC的Ksp表达式不相似,无法比价其溶解度大小,故C错误;
D、AB2与AC的Ksp表达式不相似,无法比价其溶解度大小,故D正确,
故选AD.
点评 本题主要考查的是沉淀溶解平衡和溶度积常数的计算应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
13.下列指定反应的离子方程式正确的是( )
| A. | 用足量的氢氧化钠溶液吸收二氧化氮:3NO2+2OH-═2NO3-+NO+H2O | |
| B. | 用过量的氨水吸收烟道气中的SO2:SO2+2NH3•H2O=2NH4++SO32-+H2O | |
| C. | NH4Al(SO4)2溶液与过量NaOH溶液混合加热:NH4++Al3++4OH-═Al(OH)3↓+NH3↑+H2O | |
| D. | 向酸性KMnO4溶液中通入SO2:2MnO4-+5SO2+4OH-═2Mn2++5SO42-+2H2O |
14.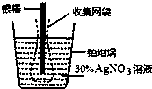 下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
 下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )| A. | 电量计工作时溶液里的阴离子向正极移动 | |
| B. | 电量计工作时银棒应与电源的正极相连 | |
| C. | 网袋是收集银溶解过程中产生的金属颗粒,若没有该网袋,测量结果会偏低 | |
| D. | 若得金属银的沉积量为1.08g,则电解过程中转移的电子为0.01mol |
3.被称为“智慧元素”--碘的单质及其化合物应用十分广泛,碘化钠常用于医疗和照相业等.某实验小组模拟其工业制备工艺流程如图1:

请回答下列问题:
(1)操作A包括加热浓缩、冷却结晶、过滤;用冰水洗涤的目的是洗涤除去表面可溶性杂质,同时尽量减少NaI的溶解损失;反应②的离子方程式为2Fe+IO3-+3H2O═2Fe(OH)3+I-.
(2)某同学推测得到的成品除含有NaI外,还可能有NaIO3和NaOH,并设计如下方案进行检验,实验结果表明其推测正确.
已知:IO3-+5I-+6H+=3I2+3H2O2;NaIO3水溶液呈中性.
限选试剂:1mol•L-1H2SO4溶液、2mol•L-1HNO3溶液、淀粉溶液、酚酞试液、石蕊试液、蒸馏水.其它仪器和用品自选.
(3)如图2装置Ⅰ为一种可充电电池的示意图,其中的离子交换膜只允许Na+通过,该电池充、放电的化学方程式为Na2S4+3NaI$?_{放电}^{充电}$2Na2S2+NaI3,装置Ⅱ为电解池的示意图.当闭合开关S时,电极X附近溶液先变红.此时,电极B上发生反应的电极反应式为NaI3+2Na++2e-=3NaI.电极Y上发生氧化(填“氧化”、“还原”)反应.装置Ⅱ溶液的体积为100mL,电解结束后若X极生成1.12L(已换算成标准状况)气体,则此时溶液的pH=14(假设溶液体积没有变化).

请回答下列问题:
(1)操作A包括加热浓缩、冷却结晶、过滤;用冰水洗涤的目的是洗涤除去表面可溶性杂质,同时尽量减少NaI的溶解损失;反应②的离子方程式为2Fe+IO3-+3H2O═2Fe(OH)3+I-.
(2)某同学推测得到的成品除含有NaI外,还可能有NaIO3和NaOH,并设计如下方案进行检验,实验结果表明其推测正确.
已知:IO3-+5I-+6H+=3I2+3H2O2;NaIO3水溶液呈中性.
限选试剂:1mol•L-1H2SO4溶液、2mol•L-1HNO3溶液、淀粉溶液、酚酞试液、石蕊试液、蒸馏水.其它仪器和用品自选.
| 实验方案 | 实验现象 | 结论 |
| 将白色晶体溶于水,并滴2滴淀粉溶液 | 得到无色溶液 | |
| 取少量溶液于试管A中,加入足量的1mol•L-1H2SO4 | 溶液呈蓝色 | 溶液中含IO3- |
| 另取少量溶液于试管B中,滴入几滴酚酞溶液 | 溶液变红 | 溶液中含大量OH- |
10.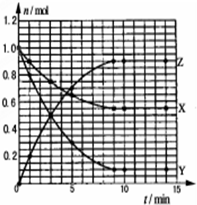 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )
 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )| A. | 反应的化学方程式是X+2Y?2Z | |
| B. | 该反应在0-3min时间内产物Z的平均反应速率0.083mol•L-1•min-1 | |
| C. | 由图象知该反应吸收能量 | |
| D. | 其他条件不变,升高温度,若正反应速率增大,则逆反应速率将减小 |
7.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 15g甲基(-CH3)所含有的电子数是10NA | |
| B. | 常温常压下,30g甲醛所含有的原子数目为4NA | |
| C. | 标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22.4 NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为12NA |
8.下列措施能减慢化学反应速率的是( )
| A. | 将煤块粉碎后燃烧 | |
| B. | 用粗锌替代纯锌与同浓度同体积的盐酸反应制氢气 | |
| C. | 将食物贮藏在冰箱中 | |
| D. | 用双氧水溶液制氧气时添加少量二氧化锰粉末 |
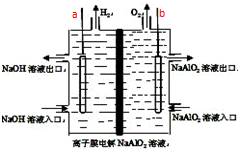 工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极):该电池的总反应方程式为:4NaAlO2+10H2O$\frac{\underline{\;通电\;}}{\;}$ 4Al(OH)3↓+4NaOH+O2↑+2H2↑.电解池阳极室发生的电极反应式是4AlO2-+6H2O-4e-=4Al(OH)3↓+O2↑,该离子膜为阳离子交换膜(填“阴”或“阳”)
工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极):该电池的总反应方程式为:4NaAlO2+10H2O$\frac{\underline{\;通电\;}}{\;}$ 4Al(OH)3↓+4NaOH+O2↑+2H2↑.电解池阳极室发生的电极反应式是4AlO2-+6H2O-4e-=4Al(OH)3↓+O2↑,该离子膜为阳离子交换膜(填“阴”或“阳”)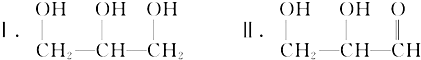
 .
.