题目内容
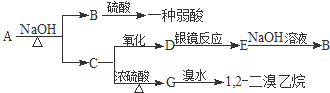
15.德国化学家列培是乙炔高压化学的开拓者,他发现了一系列乙炔的高压反应(被称为列培反应),为有机合成工业作出了巨大的贡献.部分列培反应如下(条件从略):A.HC≡CH+ROH-→CH2=CHOR
B.HC≡CH+HCHO-→HC≡CCH2OH
C.R2NCH2OH+HC≡CH-→R2NCH2C≡CH+H2O
D.R2NH+HC≡CH-→R2NCH=CH2
(1)以上反应中属于加成反应的有(填序号)ABD
(2)如图,该高聚物用途十分广泛,涉及到化妆品乳化剂、染料的分散剂、酒类的澄清剂等.试完成下列问题:
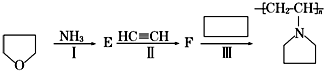
①结构简式:E
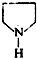 ,F
,F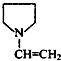
②反应类型:Ⅰ取代反应,Ⅱ加成反应.
分析 (1)比较反应中的反应物和生成物可知,A为加成反应,B为加成反应,C为取代反应,D为加成反应;
(2)根据题中各物质转化关系,反应Ⅲ为F发生加聚反应得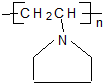 ,所以F为
,所以F为 ,依据R2NH+HC≡CH→R2NCH=CH2反应特征,反应Ⅱ为E发生加成反应生成F,所以E为
,依据R2NH+HC≡CH→R2NCH=CH2反应特征,反应Ⅱ为E发生加成反应生成F,所以E为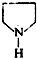 ,
,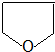 与氨气发生取代反应生成
与氨气发生取代反应生成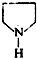 ,据此答题.
,据此答题.
解答 解:(1)比较反应中的反应物和生成物可知,A为加成反应,B为加成反应,C为取代反应,D为加成反应,
故答案为:ABD;
(2)根据题中各物质转化关系,反应Ⅲ为F发生加聚反应得 ,所以F为
,所以F为 ,依据R2NH+HC≡CH→R2NCH=CH2反应特征,反应Ⅱ为E发生加成反应生成F,所以E为
,依据R2NH+HC≡CH→R2NCH=CH2反应特征,反应Ⅱ为E发生加成反应生成F,所以E为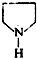 ,
, 与氨气发生取代反应生成
与氨气发生取代反应生成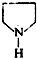 ,
,
①根据上面的分析可知,E的结构简式为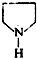 ,F为
,F为 ,
,
故答案为: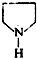 ;
; ;
;
②根据上面的分析可知,反应I的反应类型为取代反应,Ⅱ为加成反应,
故答案为:取代反应;加成反应.
点评 本题考查有机物的合成,为高考常见题型,题目侧重于有机物质的转化关系分析和反应条件的应用,准确理解题中信息是解题关键,题目难度中等,注重对基础知识和基本能力的考查.

练习册系列答案
相关题目
3.在光照条件下,CH4与Cl2能发生取代反应.若将1mol CH4与Cl2反应,待反应完成后测得四种有机取代物的物质的量之比为n(CH3Cl):n(CH2Cl2):n(CHCl3):n(CCl4)=1:2:3:4,则消耗的Cl2为( )
| A. | 1.0 mol | B. | 2.0 mol | C. | 3.0 mol | D. | 4.0 mol |
10.哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下发生反应:N2+3H2?2NH3.下列有关说法不正确的是( )
| A. | 若2分钟达到化学平衡时N2还剩下0.4mol,则v(N2)=0.3mol/(L•min) | |
| B. | 达到化学平衡时,单位时间内每生成0.1mol的H2同时生成0.1mol的NH3 | |
| C. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| D. | 达到化学平衡后,若增大压强使容器体积缩小,化学反应速率将会增大 |
20.下列关于两种有机化合物A和B的说法中错误的是( )
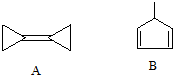

| A. | A的化学式为C6H8 | B. | A的二氯取代产物有4种 | ||
| C. | A与B与溴水反应产物都只有一种 | D. | A分子所有碳原子均在同一平面上 |
4.下列装置所示的实验能达到实验目的是( )
| A. |  分离碘酒中 的碘和酒精 | B. | 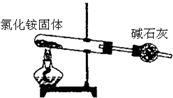 实验室制取氨气 | ||
| C. | 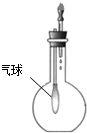 验证NH3的 溶解性 | D. | 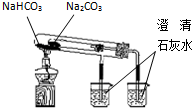 比较Na2CO3、NaHCO3的热稳定性 |
5.已知1-18号元素的离子aW3+、bX+、CY2-、dZ-都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A. | 四种元素位于同一周期 | B. | 氢化物的稳定性H2Y>HZ | ||
| C. | X与Y形成的化合物中必有离子键 | D. | 原子半径Z>Y |