题目内容
18.关于氢键,下列说法正确的是( )| A. | 每一个水分子内含有两个氢键 | |
| B. | 冰、水和水蒸气中都存在氢键 | |
| C. | 分子间形成的氢键使物质的熔点和沸点升高 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
分析 A.水分子内不存在氢键;
B.水蒸气分子之间不形成氢键;
C.分子间形成的氢键使物质的熔点和沸点升高;
D.氢键只影响物理性质,与化学性质无关.
解答 解:A.水分子内不含氢键,只存在与水分子之间,故A错误;
B.水蒸气中水分子距离较大,不形成氢键,故B错误;
C.分子间形成的氢键使物质的熔点和沸点升高,故C正确;
D.H2O是一种非常稳定的化合物,与共价键有关,与氢键无关,故D错误.
故选C.
点评 本题考查氢键的形成与性质,题目难度不大,注意氢键与分子间作用力、化学键的区别,易错点为氢键对物质性质的影响.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
9.下表为元素周期表的一部分,用元素符号或化学式回答下列问题.
(1)10种元素中,化学性质最不活泼的是Ar,除⑩外原子半径最大的是K.
(2)①②⑤三种元素最高价氧化物对应的水化物碱性最强的是KOH
(3)①②③④⑤⑧六种元素形成的离子半径由大到小的顺序为Cl->K+>Ca2+>Na+>Mg2+>Al3+
(4)元素⑦的氢化物的化学式为H2O;该氢化物和元素②单质反应的化学方程式为2K+2H2O=2KOH+H2↑.
(5)①⑨形成的化合物灼烧时火焰焰色为黄色;该化合物的溶液与元素⑧的单质反应的化学方程式为Cl2+2NaBr=2NaCl+Br2 .
(6)①、⑤和⑧最高价氧化物对应水化物间相互反应的离子方程式Al(OH)3+3H+═Al3++2H2O、Al(OH)3+OH-═AlO2-+2H2O、H++OH-=H2O.
(7)③的单质在⑥⑦形成化合物中燃烧的化学方程式为CO2+2Mg$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;单质⑨溶入⑥⑧形成化合物所得溶液的颜色为橙红色;⑦⑧⑨形成氢化物的稳定性由强到弱顺序为H2O>HCl>HBr.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①②⑤三种元素最高价氧化物对应的水化物碱性最强的是KOH
(3)①②③④⑤⑧六种元素形成的离子半径由大到小的顺序为Cl->K+>Ca2+>Na+>Mg2+>Al3+
(4)元素⑦的氢化物的化学式为H2O;该氢化物和元素②单质反应的化学方程式为2K+2H2O=2KOH+H2↑.
(5)①⑨形成的化合物灼烧时火焰焰色为黄色;该化合物的溶液与元素⑧的单质反应的化学方程式为Cl2+2NaBr=2NaCl+Br2 .
(6)①、⑤和⑧最高价氧化物对应水化物间相互反应的离子方程式Al(OH)3+3H+═Al3++2H2O、Al(OH)3+OH-═AlO2-+2H2O、H++OH-=H2O.
(7)③的单质在⑥⑦形成化合物中燃烧的化学方程式为CO2+2Mg$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;单质⑨溶入⑥⑧形成化合物所得溶液的颜色为橙红色;⑦⑧⑨形成氢化物的稳定性由强到弱顺序为H2O>HCl>HBr.
6.将如图所示实验装置的K闭合,下列判断正确的是( )
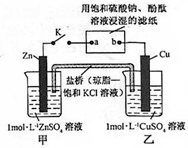

| A. | 片刻后甲池中c(SO42-)增大 | B. | 电子沿 Zn→a→b→Cu 路径流动 | ||
| C. | Cu 电极上发生还原反应 | D. | 片刻后可观察到滤纸b点变红色 |
3.有关卤代烃的说法正确的是( )
| A. | CH2=CHBr属于卤代烃 | |
| B. | 卤代烃密度都大于水 | |
| C. | 卤代烃都会水解生成醇 | |
| D. | 卤代烃都能和NaOH醇溶液发生消去反应 |
10.下列涉及有机物的性质或应用的说法不正确的是( )
| A. | 甲醛是一种有刺激性气味的气体 | |
| B. | 石油通过裂解可以得到更多的汽油,可以满足工业需求 | |
| C. | 乙醇易溶于水是因为含有羟基 | |
| D. | 氟氯代烷产生的自由基可以作为催化剂使O3转化为O2,从而破坏臭氧层 |
7.铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期.Tl3+与Ag在酸性介质中发生反应:Tl3++2Ag=Tl++2Ag+.下列推断正确的是( )
| A. | Tl(OH)3是两性氢氧化物 | B. | Tl3+的氧化性比Al3+强 | ||
| C. | Tl 能形成+3价和+1价的化合物 | D. | Tl+的还原性比Ag强 |
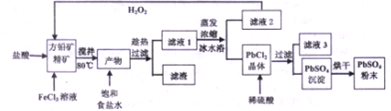
 ”表示)位于该正方体的顶点或面心;阴离子(用“
”表示)位于该正方体的顶点或面心;阴离子(用“ ”表示)位于小正方体的中心.根据以上信息,回答下列问题:A至E的元素名称:
”表示)位于小正方体的中心.根据以上信息,回答下列问题:A至E的元素名称: